题目内容
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、标准状况下,22.4L CH3CHO中含有的分子数为NA |
| B、pH=1的稀硫酸中含有的H+数为0.1NA |
| C、7.80g Na2O2与5.85g NaCl所含阴离子数相等 |
| D、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.标准状况下,乙醛不是气体,不能使用标况下的气体摩尔体积计算乙醛的物质的量;
B.缺少稀硫酸的体积,无法计算溶液中氢离子的数目;
C.过氧化钠中的阴离子为过氧根离子,7.8g过氧化钠的物质的量为0.1mol,含有0.1mol阴离子,5.85g氯化钠的物质的量为0.1mol,含有0.1mol氯离子;
D.氯气溶于水,只有部分氯气与水反应生成氯化氢和次氯酸.
B.缺少稀硫酸的体积,无法计算溶液中氢离子的数目;
C.过氧化钠中的阴离子为过氧根离子,7.8g过氧化钠的物质的量为0.1mol,含有0.1mol阴离子,5.85g氯化钠的物质的量为0.1mol,含有0.1mol氯离子;
D.氯气溶于水,只有部分氯气与水反应生成氯化氢和次氯酸.
解答:
解:A.标况下,乙醛不是气体,题中条件无法计算22.4L乙醛的物质的量,故A错误;
B.没有告诉稀硫酸的体积,无法计算溶液中氢离子的物质的量及数目,故B错误;
C.7.80g过氧化钠的物质的量为0.1mol,0.1mol过氧化钠中含有0.1mol阴离子过氧根离子,5.85g氯化钠中含有0.1mol氯化钠,含有0.1mol氯离子,二者含有的阴离子的物质的量都是0.1mol,含有的阴离子数目相等,故C正确;
D.0.1mol氯气溶于水,只有少量的氯气与水反应生成氯化氢和次氯酸,所以转移的电子的物质的量小于0.1mol,转移的电子数目小于0.1NA,故D错误;
故选C.
B.没有告诉稀硫酸的体积,无法计算溶液中氢离子的物质的量及数目,故B错误;
C.7.80g过氧化钠的物质的量为0.1mol,0.1mol过氧化钠中含有0.1mol阴离子过氧根离子,5.85g氯化钠中含有0.1mol氯化钠,含有0.1mol氯离子,二者含有的阴离子的物质的量都是0.1mol,含有的阴离子数目相等,故C正确;
D.0.1mol氯气溶于水,只有少量的氯气与水反应生成氯化氢和次氯酸,所以转移的电子的物质的量小于0.1mol,转移的电子数目小于0.1NA,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项C为易错点,注意过氧化钠中阴离子为过氧根离子.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
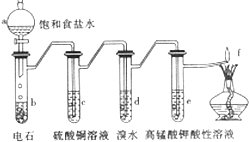 如图是制备和研究乙炔性质的实验装置图.下列说法不正确的是( )
如图是制备和研究乙炔性质的实验装置图.下列说法不正确的是( )| A、制备乙炔的反应原理是:CaC2+2H2O→Ca(OH)2+C2H2↑ |
| B、c的作用是除去影响后续实验的杂质 |
| C、d中的有机产物与AgNO3溶液混合能产生沉淀 |
| D、e中的现象说明乙炔能被高锰酸钾酸性溶液氧化 |
下列说法正确的是( )
| A、温室效应是当今世界面临的环境问题,使温室效应增强的气体只有二氧化碳 |
| B、直馏汽油、裂化汽油、植物油、甘油均能与溴发生加成反应而使溴的四氯化碳溶液褪色 |
| C、PX(对二甲苯)是制造聚酯纤维的原料,它是一种难溶于水密度比水大的剧毒物质 |
| D、晶体硅可用于制作太阳能电池板,二氧化硅可用于制作光导纤维 |
室温下,有pH均为9体积均为10mL的NaOH溶液和CH3COONa溶液,下列说法正确的是( )
| A、两种溶液中的c(Na+)相等 | ||
B、两溶液中由水电离出的c(OH-)之比为
| ||
| C、分别加水稀释到100mL时,两种溶液的pH依然相等 | ||
| D、分别与同浓度的盐酸反应,恰好反应时消耗的盐酸体积相等 |
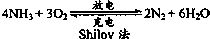 以氨气代替氢气来研发氨燃料电池是当前科研的一个热点.氨燃料电池使用的电解质溶液是KOH溶液,电池反应如图:有关下列说法错误的是( )
以氨气代替氢气来研发氨燃料电池是当前科研的一个热点.氨燃料电池使用的电解质溶液是KOH溶液,电池反应如图:有关下列说法错误的是( )| A、氨燃料电池在充电时,OH-向电池的负极移动 |
| B、氨燃料电池在放电时,负极反应为:2NH3-6e-+6OH-═N2+6H2O |
| C、以氨气代替氢气的主要原因是:氨气易液化易储存 |
| D、燃料电池的能量转化率一般比普通的电池高 |
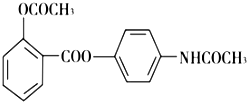 贝诺酯具有抗风湿、解热镇痛作用,其结构简式如图,下列说法正确的是( )
贝诺酯具有抗风湿、解热镇痛作用,其结构简式如图,下列说法正确的是( )| A、贝诺酯可与水任意比互溶 |
| B、贝诺酯完全水解后能得到3种物质 |
| C、1mol贝诺酯最多可与9mol H2发生加成反应 |
| D、贝诺酯可发生取代反应、消去反应和聚合反应 |
下列说法不正确的是( )
| A、分子式为CH4O和C2H6O的物质不一定互为同系物 |
| B、通过乙烷的取代反应或乙烯的加成反应都可以制取纯净的氯乙烷 |
| C、淀粉.纤维素都属于糖类,它们通式相同,但它们不互为同分异构体 |
| D、某有机化合物仅由C.H.O三种元素组成,其相对分子质量小于150,若已知其中氧的质量分数为50%,则分子中碳原子的个数最多为5 |
下列各组离子在水溶液中能大量共存的是( )
| A、Na+、HCO3-、SO32-、OH- |
| B、Al3+、H+、SiO32-、I- |
| C、Fe2+、K+、NO3-、SO42- |
| D、Fe3+、NH4+、ClO-、CO32- |

