题目内容
适量的下列物质中,不能使湿润的淀粉碘化钾试纸变蓝的是( )
| A、氯水 | B、碘水 |
| C、溴水 | D、二氧化硫气体 |
考点:氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:能使湿润的淀粉-碘化钾试纸变蓝,选项中的物质应具有氧化性,且氧化性大于碘或存在碘单质;反之,不具有氧化性或氧化性比碘的弱,则不能使湿润的淀粉-碘化钾试纸变蓝,以此来解答.
解答:
解:A.氯水与KI反应生成碘,能使湿润的淀粉-碘化钾试纸变蓝,故A不选;
B.碘水中含碘单质,遇淀粉变蓝,则能使湿润的淀粉-碘化钾试纸变蓝,故B不选;
C.溴水与KI反应生成碘,能使湿润的淀粉-碘化钾试纸变蓝,故C不选;
D.二氧化硫与碘化钾不反应,不能使试纸变蓝,故D选.
故选D.
B.碘水中含碘单质,遇淀粉变蓝,则能使湿润的淀粉-碘化钾试纸变蓝,故B不选;
C.溴水与KI反应生成碘,能使湿润的淀粉-碘化钾试纸变蓝,故C不选;
D.二氧化硫与碘化钾不反应,不能使试纸变蓝,故D选.
故选D.
点评:本题考查碘的特征反应及氧化还原反应,明确氧化性的强弱及碘遇淀粉变蓝是解答本题的关键,注意选项B中含碘单质,题目难度不大.

练习册系列答案
相关题目
能正确表示下列化学反应的离子方程式是( )
| A、用氢氧化钠溶液吸收少量二氧化硫:2OH-+SO2═SO32-+H2O |
| B、金属铝溶于盐酸中:Al+2H+═Al3++H2↑ |
| C、硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ |
| D、碳酸镁溶于硝酸中:CO32-+2H+═H2O+CO2↑ |
下列气体:①Cl2 ②SO2 ③NO2 ④NH3 ⑤H2S ⑥H2不能用浓硫酸干燥的是( )
| A、只有④ | B、④⑤ |
| C、②④⑤⑥ | D、全部 |
下列关于葡萄糖的说法错误的是( )
| A、葡萄糖的分子式是C6H12O6 |
| B、葡萄糖属于单糖 |
| C、葡萄糖是碳水化合物,因为它的分子是由6个碳原子和6个水分子组成 |
| D、葡萄糖能与新制的氢氧化铜悬浊液共热反应,生成砖红色的沉淀 |
下列物质肯定是纯净物的是( )
| A、天然气 |
| B、分子式为C2H6O的物质 |
| C、聚甲基丙烯酸甲酯 |
| D、分子式为C2H5Cl的物质 |
在无色透明的强酸性溶液中,能大量共存的离子组是( )
| A、K+、Na+、NO3-、MnO4- |
| B、Mg2+、Na+、Cl-、SO42- |
| C、K+、Cu2+、Br-、S2- |
| D、NH4+、Al3+、I-、NO3- |
 某污水中含有Fe3+、Ag+、Cu2+等离子,某工厂采用电解的方法处理该污水,具体的做法是:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3.Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用,阴极产生的气泡把污水中悬浮物带到水面形成浮层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.该厂污水处理设计装置如图所示,下列说法正确的是( )
某污水中含有Fe3+、Ag+、Cu2+等离子,某工厂采用电解的方法处理该污水,具体的做法是:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3.Fe(OH)3具有吸附性,可吸附污物而沉积下来,有净化水的作用,阴极产生的气泡把污水中悬浮物带到水面形成浮层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.该厂污水处理设计装置如图所示,下列说法正确的是( )| A、通入空气的电极为阳极 |
| B、甲装置中Fe电极的反应为Fe-3e-═Fe3+ |
| C、为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时,循环物质为CO2 |
| D、当乙装置中有1.6 g CH4参加反应,则C电极理论上生成气体在标准状况下为8.96 L |
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
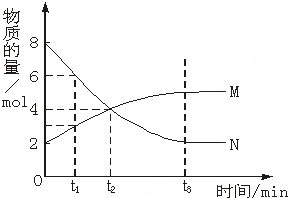

| A、反应的化学方程式为:M?N |
| B、t2时,正逆反应速率相等,达到平衡 |
| C、t3时,正反应速率大于逆反应速率 |
| D、t1时,N的浓度是M浓度的2倍 |
在固定体积的密闭容器中进行如下反应:2SO2(g)+O2(g)?2SO3(g).已知反应过程某一时刻SO2、O2、SO3浓度(mol/L)分别为0.2、0.1、0.2,达到平衡时,浓度可能正确的是( )
| A、SO2为0.25mol/L |
| B、SO2,O2分别为0.4,0.2mol/L |
| C、SO2,SO3均为0.15mol/L |
| D、SO3为0.4mol/L |