题目内容
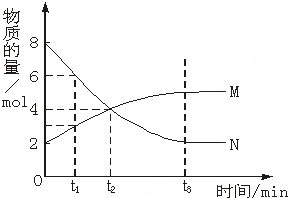
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )

| A、反应的化学方程式为:M?N |
| B、t2时,正逆反应速率相等,达到平衡 |
| C、t3时,正反应速率大于逆反应速率 |
| D、t1时,N的浓度是M浓度的2倍 |
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:达到平衡时,N的物质的量为2mol,变化量为6mol,M的物质的量为5mol,变化量为3mol,反应的方程式为2N?M,结合图象解答该题.
解答:
解:A、达到平衡时,N的物质的量为2mol,变化6mol,M的物质的量为5mol,变化3mol,反应的方程式为2N?M,故A错误;
B、t2时,M、N的物质的量还在变化,没有达到平衡状态,则正逆反应速率不等,故B错误;
C、t3时,M、N的物质的量不在变化,达到平衡状态,则正逆反应速率相等,故C错误;
D、t1时,N的物质的量为6mol,M的物质的量为3mol,则N的浓度是M浓度的2倍,故D正确.
故选:D.
B、t2时,M、N的物质的量还在变化,没有达到平衡状态,则正逆反应速率不等,故B错误;
C、t3时,M、N的物质的量不在变化,达到平衡状态,则正逆反应速率相等,故C错误;
D、t1时,N的物质的量为6mol,M的物质的量为3mol,则N的浓度是M浓度的2倍,故D正确.
故选:D.
点评:本题考查化学平衡与图象问题的考查,侧重于学生分析能力的考查,为高考常见题型,难度中等,注意把握图象曲线变化的趋势以及平衡状态的判断.

练习册系列答案
相关题目
下列说法正确的是( )
| A、欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)为:中和滴定实验、pH试纸 |
| B、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
| C、C3H2Cl6的六氯代物共有4种,而且CH3-CH=CH-CH3与C3H6一定互为同系物 |
| D、.将0.1 mol/L的NaOH溶液与0.5 mol/L的CuSO4溶液等体积混合制得氢氧化铜悬浊液,用于检验麦芽糖是还原糖 |
适量的下列物质中,不能使湿润的淀粉碘化钾试纸变蓝的是( )
| A、氯水 | B、碘水 |
| C、溴水 | D、二氧化硫气体 |
水的电离过程为H2O?H++OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14,KW(35℃)=2.1×10-14.则下列叙述正确的是( )
| A、c(H+)随温度的升高而降低 |
| B、35℃时,c(H+)>c(OH-) |
| C、溶液:pH(35℃)>pH(25℃) |
| D、水的电离是吸热的过程 |
下列烷烃在光照下与氯气反应,生成3种二氯代烃的是( )
| A、CH3CH2CH2CH3 |
B、 |
C、 |
D、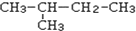 |
下列金属冶炼的反应原理,错误的是( )
A、2NaCl(熔融)
| ||||
B、MgO+H2
| ||||
C、Fe3O4+4CO
| ||||
D、2HgO
|
关于如图所示装置的叙述,正确的是( )


| A、氢离子在铜片表面被还原 |
| B、铜片质量逐渐减少 |
| C、电流从锌片经导线流向铜片 |
| D、铜是负极,铜片上有气泡产生 |
 某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白: