题目内容
12.下有机物A的分子式为C4H10O,则A的结构可能有(不含对映异构)( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
分析 有机物A的分子式为C4H10O,可能为醚,也可能为醇,若为醚,根据可能的烃基进行组合判断同分异构体,若为醇,看作丁烷中H原子被-OH确定,丁烷有正丁烷、异丁烷,利用等效氢判断丁醇同分异构体数目.
解答 解:有机物A的分子式为C4H10O,可能为醚,也可能为醇.
若为醚,可以是CH3OCH2CH2CH3、CH3OCH(CH3)2、CH3CH2OCH2CH3,
若为醇,看作丁烷中H原子被-OH确定,丁烷有正丁烷、异丁烷,分别有2种氢原子,可以得到4种醇,
故符合条件的同分异构体共有7种,
故选:D.
点评 本题考查同分异构体书写,侧重考查学生分析推理能力,注意利用取代法与等效氢确定丁醇同分异构体.

练习册系列答案
相关题目
2.控制适宜的条件,将反应2Fe3++2Iˉ?2Fe2++I2设计成如图所示的原电池.下列判断 错误的是( )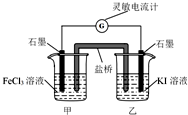

| A. | 反应开始时,乙中石墨电极上发生氧化反应 | |
| B. | 反应开始时,甲中石墨电极为正极 | |
| C. | 电流计读数为零时,反应达到化学平衡状态 | |
| D. | 电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极 |
3. 在一恒温恒压的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示.下列说法不正确的是( )
在一恒温恒压的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示.下列说法不正确的是( )
 在一恒温恒压的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示.下列说法不正确的是( )
在一恒温恒压的密闭容器中发生如下反应:A(g)+B(g)?2C(g)△H<0,t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图所示.下列说法不正确的是( )| A. | 0~t2时,v(正)>v(逆) | |
| B. | Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ=Ⅱ | |
| C. | t2时刻改变的条件是向密闭容器中加C | |
| D. | Ⅰ、Ⅱ两过程达到平衡时,平衡常数K(Ⅰ)=K(Ⅱ) |
20.将NaHCO3和Na2O2的固体混合物x g在密闭容器中加热至250℃,充分反应后排出气体.将反应后的固体溶入水无气体放出,再逐滴加入盐酸,产生气体(标准状况)与所加盐酸体积之间的关系如图所示.下列说法错误的是( )

| A. | HCl的浓度0.2mol/L | |
| B. | 反应后固体的成分为NaOH与Na2CO3 | |
| C. | 密闭容器中排出气体的成分为O2和H2O | |
| D. | x的数值为6.09 |
7.已知${\;}_{17}^{35}$Cl的相对原子质量为34.969,下列相关说法正确的是( )
| A. | 氯元素的近似相对原子质量为35 | B. | 氯元素的某种同位素的质量数为35 | ||
| C. | 氯元素的中子数为18 | D. | 氯原子的质量为34.969 |
17.以0.10mol/L的氢氧化钠溶液滴定某一元酸HA的滴定曲线如图所示.下列表述正确的是( )


| A. | 此实验可以选用甲基橙作指示剂 | |
| B. | 该酸HA的浓度约为1×10-4mol/L | |
| C. | 当NaOH体积为9 mL时,恰好完全中和反应 | |
| D. | 达到滴定终点时,溶液中c(Na+)>c (A-) |