题目内容
6.等温、等压下,同体积的A、B两种气体的质量比为23:16,若B的相对分子质量为32,则A的化学式为( )| A. | NO2 | B. | NO | C. | N2O3 | D. | N2O5 |
分析 等温、等压下,同体积的A、B两种气体的物质的量相等,而质量比为23:16,B的相对分子质量为32,所以A的相对分子质量为:32×2=46,由此分析解答.
解答 解:等温、等压下,同体积的A、B两种气体的物质的量相等,而质量比为23:16,B的相对分子质量为32,所以A的相对分子质量为:32×2=46,则化学式为:NO2,故选A.
点评 本题考查阿伏伽德罗定律及其推论,明确体积、质量和摩尔质量之间的关系是解本题的关键,难度不大.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
17.下列说法正确的是( )
| A. | H2、D2、T2属于同位素 | |
| B. | 氯水、氨水、王水是混合物,水银、水玻璃是纯净物 | |
| C. | 水能、风能、生物质能是可再生能源,煤、石油是不可再生能源 | |
| D. | HCl、NH3、BaSO4是电解质,CO2、Cl2、CH3CH2OH不是电解质 |
14.下列说法正确的是( )
| A. | 陈年老酒的香气浓是因为乙醇的特殊的香气 | |
| B. | 钠与乙醇的反应比钠与水的反应激烈,发生了取代反应 | |
| C. | 乙烯是重要的化工原料,乙烯的产量可以用来衡量一个国家的石油化工水平 | |
| D. | 乙烯分子所有原子都在同一平面上,丙烯也是 |
1.下列说法不正确的是( )
| A. | Na2O的熔点高于K2S,是因为Na2O晶格能大 | |
| B. | 共用电子对不发生偏移的共价键是非极性键 | |
| C. | Na、Mg、Al第一电离能大小顺序:Na<Mg<Al | |
| D. | HCl极易溶于水,是因为它们的分子均为极性分子 |
1.J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的元素.
下列说法错误的是( )
| J | ||||
| R |
| A. | J的单质一定能导电 | |
| B. | J、R形成的化合物JR2中J与R原子间是极性共价键 | |
| C. | R、T两元素的气态氢化物中,T的气态氢化物更稳定 | |
| D. | 四种元素中T的最高价氧化物的水化物酸性最强 |
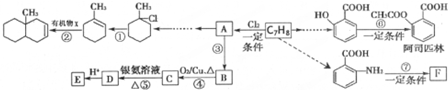
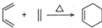 ②
②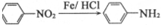
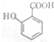 可选用的试剂有bd(填标号)
可选用的试剂有bd(填标号)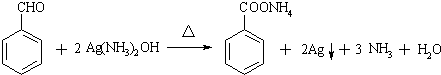 .
.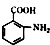 的合成路线流程图(无机试剂任用)合成路线流程图示例如下:CH2═CH2$→_{催化剂,△}^{H_{2}O}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}COOH}$CH3COOCH2CH3.
的合成路线流程图(无机试剂任用)合成路线流程图示例如下:CH2═CH2$→_{催化剂,△}^{H_{2}O}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}COOH}$CH3COOCH2CH3. 硫化钠
硫化钠 氢氧化钠
氢氧化钠
 氮气
氮气 次氯酸
次氯酸 .
.