题目内容
欲配制480mL 0.2mol/L的NaCl溶液,回答下列问题:
(1)应用托盘天平准确称取固体NaCl g。
(2)以下是实验操作步骤,正确的操作顺序是:
①称取所需质量的NaCl
②将溶液转移到容量瓶内
③用蒸馏水洗涤烧杯2~3次,将洗涤液全部移入容量瓶中,摇匀
④改用胶头滴管,小心滴入蒸馏水至刻度
⑤仔细地把蒸馏水注入容量瓶中,直到液面接近刻度线1cm~2cm处
⑥塞上瓶塞,反复上下颠倒,摇匀
⑦将称取的NaCl固体,加适量蒸馏水,搅拌溶解后冷却
(3)若实验遇到下列情况,所配制的溶液浓度偏小的操作是
| A.烧杯中NaCl溶液移入容量瓶后没有洗涤烧杯 |
| B.定容后摇匀,发现液面低于刻度线,再滴加蒸馏水至刻度线 |
| C.实验用的容量瓶洗净后未干燥,里面含有少量水 |
| D.定容时俯视 |
(7分)
(1)5.9 (2分)(2) ①⑦②③⑤④⑥(3分) (3)AB(2分)
解析试题分析:(1)欲配制480mL 0.2mol/L的NaCl溶液,则应配制500mL0.2mol/L的NaCl溶液,所以氯化钠的质量是0.5L×0.2mol/L×58.5g/mol=5.85g,根据托盘天平的精确度,所以只能称取5.9g的NaCl;
(2)用固体配制溶液的步骤是:称取氯化钠的质量、在烧杯中溶解、冷却后移入容量瓶、洗涤烧杯、玻璃棒2-3次并将洗涤液移入容量瓶、摇匀,使溶液均匀、直接把蒸馏水注入容量瓶中,至液面接近刻度线1cm~2cm处,改用胶头滴管加水,定容、盖上瓶塞上下颠倒,反复摇匀、装瓶。所以正确 操作顺序是①⑦②③⑤④⑥;
(3)A、未洗涤烧杯,造成氯化钠质量减少,所配溶液的浓度偏小,正确;B、定容后又加水,则溶液的体积偏大,溶液浓度偏小,正确;C、在配制的过程中,需直接加入蒸馏水,所以容量瓶内有少量蒸馏水,对结果无影响,错误;D、定容时俯视刻度线,使所配溶液的体积偏小,浓度偏大,错误,答案选AB。
考点:考查溶液的配制步骤的判断,误差的分析

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案化学与人类生活、社会可持续发展密切相关,下列措施有利于节能减排、保护环境的是
①加快化石燃料的开采与使用;②研发易降解的生物农药;③应用高效洁净的能源转化技术;
④田间焚烧秸秆;⑤推广使用节能环保材料。
| A.①③⑤ | B.②③⑤ | C.①②④ | D.②④⑤ |
(10分)某同学帮助水质检测站配制800mL 1 mol·L-1NaOH溶液备用。
(1)该同学应选择的玻璃仪器除了烧杯、量筒、玻璃棒、胶头滴管外,还有 。
(2)其操作步骤如下图所示,则如图操作应在下图中的 (填选项字母)之间。
| A.②与③ | B.①与② | C.④与⑤ | D.③与④ |

(3)该同学应用托盘天平称取NaOH固体 g,用质量为33.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在下图中选出能正确表示游码位置的选项 (填选项字母)。

(4)下列操作对所配溶液浓度大小有何影响 (填“偏大”、“偏小”或“无影响”)。
①定容时,仰视读数,浓度会 ;
②转移溶液过程中,未洗涤玻璃棒和烧杯,浓度会 ;
③容量瓶未干燥,浓度会 ;
④定容摇匀后发现溶液凹面低于刻度线,继续加水至刻度线,浓度会 。
(5)配制溶液的实际操作过程中,动作要快,否则由于 ,会使配制的NaOH溶液的浓度比1 mol·L-1______(填“大”或“小”)。
(10分)某同学帮助水质检测站配制480 mL 0.5 mol·L-1 NaOH溶液以备使用。
(1)该同学应选择________mL的容量瓶。
(2)其操作步骤如下图所示,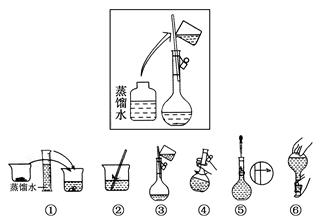
则如图操作应在下图中的________(填选项字母)之间。
A.②与③ B.①与② C.④与⑤
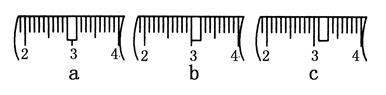
(3)该同学应称取NaOH固体________g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小________(填字母),并在下图中选出能正确表示游码位置的选项________(填字母)。
附表 砝码规格
| | a | b | c | d | e |
| 砝码大小/g | 100 | 50 | 20 | 10 | 5 |
(4)下列操作对所配溶液的浓度大小有何影响?
①转移完溶液后未洗涤玻璃棒和烧杯,浓度会________(填“偏大”、“偏小”或“无影响”,下同)
②容量瓶中原来有少量蒸馏水,浓度会________。
(8分)某学生用已准确称量的2.000g烧碱固体配制一定物质的量浓度的溶液500mL。实验室提供以下仪器:
①100mL烧杯 ②100 mL量筒 ③1000 mL容量瓶 ④500 mL容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码)。
请回答下列问题:
(1)配制时,必须使用的仪器有_________(填代号),还缺少的仪器是 (填仪器名称);
(2)配制时正确的操作顺序是(字母表示,每个操作只用一次) ;
| A.用少量水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡 |
| B.在盛有NaOH固体的烧杯中加入适量水溶解 |
| C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中 |
| D.将容量瓶盖紧,反复上下颠倒,摇匀 |
F.继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(3)实验中两次用到玻璃棒,其作用分别是:先用于______ _ _,后用于___ _____ ;
(4)若出现如下情况,其中将引起所配溶液浓度偏高的是 ;(填下列编号)
①容量瓶实验前用蒸馏水洗干净,但未烘干
②定容观察液面时俯视
③配制过程中遗漏了(2)中步骤A
(5)计算:该烧碱溶液的物质的量浓度为 。
(每空2分,共12分)
用质量分数为37.5%的浓盐酸(密度为1.16g/cm3)配制成1mol/L的稀盐酸。现实验室仅需要这种盐酸220mL。试回答下列问题:
(1)配制稀盐酸时,应选用容量为 mL的容量瓶;
(2)经计算需要量取 mL浓盐酸,在量取时宜选用下列量筒中的 。
| A.5 mL | B.10 mL | C.25 mL | D.50 mL |
①等稀释的盐酸其温度与室温一致后,沿玻璃棒注入容量瓶中。
②往容量瓶中小心加蒸馏水至液面接近环形标线2~3 cm处,改用胶头滴管加蒸馏水,使溶液的凹面底部与瓶颈的环形标线相切。
③ 在盛盐酸的烧杯中注入适量的蒸馏水,并用玻璃棒搅动,使其混合均匀。
④ 用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。上述操作中,正确的操作顺序为 (填序号)。
(4)在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度 (填“偏高”、“偏低”、“无影响”)。若未用蒸馏水洗涤烧杯内壁和玻璃棒或未将洗涤液注入容量瓶,则配制的稀盐酸浓度是 (填“偏高”、“偏低”、“无影响”)。
(5) 配制完后,应将容量瓶中的稀盐酸转移到干燥洁净的试剂瓶中存放,盖好塞子并贴上标签。
可用于判断碳酸氢钠固体粉末中混有碳酸钠的实验方法是
| A.加热时无气体放出 | B.溶于水后滴加稀BaCl2溶液有白色沉淀生成 |
| C.滴加盐酸时有气泡放出 | D.溶于水后滴加澄清石灰水有白色沉淀生成 |