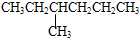题目内容
(1)在Fe3O4+4CO
3Fe+4CO2的中, 是氧化剂, 是还原剂, 元素被氧化, 元素被还原.
(2) HCl+ KMnO4═ KCl+ MnCl2+ Cl2+ H2O
氧化产物是 还原产物是 由化合价升降关系得其系数(物质的量)之比为 ;根据方程式判断氧化性是: 大于 .
| ||
(2)
氧化产物是
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)在Fe3O4+4CO
3Fe+4CO2的反应中,Fe元素化合价降低,被还原,Fe3O4为氧化剂,C元素化合价升高,被氧化,CO为还原剂;
(2)反应中Cl元素化合价升高,被氧化,Mn元素化合价降低,被还原,以此解答该题.
| ||
(2)反应中Cl元素化合价升高,被氧化,Mn元素化合价降低,被还原,以此解答该题.
解答:
解:(1)在Fe3O4+4CO
3Fe+4CO2的反应中,Fe元素化合价降低,被还原,Fe3O4为氧化剂,C元素化合价升高,被氧化,CO为还原剂,
故答案为:Fe3O4;CO;C;Fe;
(2)反应中Cl元素化合价由-1价升高到0价,被氧化,Mn元素化合价降低,由+7价降低到+2价,被还原,根据质量守恒和得失电子守恒可知配平后的方程式应为
16HCl+2KMnO4═2KCl+2MnCl2+5Cl2+8H2O,反应中为氧化产物,为还原产物,氧化产物和还原产物的物质的量之比为5:2,氧化还原反应中氧化剂氧化性大于氧化产物氧化性,则氧化性KMnO4>Cl2,
故答案为:16;2;2;2;5;8;Cl2;MnCl2;5:2; KMnO4;Cl2.
| ||
故答案为:Fe3O4;CO;C;Fe;
(2)反应中Cl元素化合价由-1价升高到0价,被氧化,Mn元素化合价降低,由+7价降低到+2价,被还原,根据质量守恒和得失电子守恒可知配平后的方程式应为
16HCl+2KMnO4═2KCl+2MnCl2+5Cl2+8H2O,反应中为氧化产物,为还原产物,氧化产物和还原产物的物质的量之比为5:2,氧化还原反应中氧化剂氧化性大于氧化产物氧化性,则氧化性KMnO4>Cl2,
故答案为:16;2;2;2;5;8;Cl2;MnCl2;5:2; KMnO4;Cl2.
点评:本题考查氧化还原反应,为高考常见题型和高频考点,侧重于学生的分析能力的考查,本题切入点是元素化合价,为解答该题的关键,难度中等.

练习册系列答案
相关题目
锌与一定量很稀的硝酸恰好完全反应生成硝酸锌、硝酸铵和水.当生成1mol硝酸锌时,被还原的硝酸与未被还原的硝酸的质量比为( )
| A、9:1 | B、8:1 |
| C、1:8 | D、1:9 |
下列物质熔沸点高低比较正确的是( )
| A、SiO2<CO2 |
| B、CCl4<CF4 |
| C、NaCl<HCl |
| D、HF>HCl |

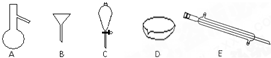
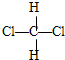 和
和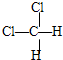 ⑦
⑦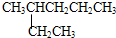 和
和