题目内容
16.实验室可以用铁片与稀硫酸反应制取氢气,下列措施不能使氢气的生成速率增大的是( )| A. | 加热 | |
| B. | 不用稀硫酸,改用质量分数为98%的浓硫酸 | |
| C. | 不用铁片改用镁条 | |
| D. | 不用铁片,改用铁粉 |
分析 增大金属与酸反应的化学反应速率,可通过增大浓度、升高温度或形成原电池反应等措施,注意浓硫酸和铁发生钝化反应,以此解答该题.
解答 解:A.温度升高,反应速率增大,故A不选;
B.改用浓硫酸溶液,浓硫酸和铁发生钝化反应,不能生成氢气,故B选;
C.镁比铁活泼,改用镁条,反应速率增大,故C不选;
D.改用铁粉,增大了反应物的接触面积,反应速率加快,故D不选.
故选B.
点评 本题考查影响化学反应速率的因素,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意浓硫酸与铁在常温下发生钝化.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
7.已知铝也能和氢氧化钠溶液反应:2Al+2NaOH+2H2O→2NaAlO2+3H2↑,现有两份铝,一份与过量的氢氧化钠溶液反应,另一份与过量的盐酸反应,若要制取等质量的氢气,则两份铝的质量比为( )
| A. | 1:1 | B. | 1:2 | C. | 2:3 | D. | 3:2 |
4.对一些具有危险的化学物质,若要在其包装上贴危险化学品标记,下列标签贴错的是( )
| A. |  浓硫酸 | B. |  汽油 | C. |  KNO3 | D. |  乙醇 |
8.下列离子方程式表达正确的是( )
| A. | 向硫酸铵溶液中滴加氢氧化钡溶液:Ba2++SO42-=BaSO4↓ | |
| B. | 钠跟水反应:Na+2H2O=Na++2OH-+H2↑ | |
| C. | AlCl3溶液中加入过量氨水:Al3++4NH3.H2O=AlO2-+4NH4++2H2O | |
| D. | 用NaOH溶液吸收少量Cl2:Cl2+2OH-=Cl-+ClO-+H2O |
6.在NO2被水吸收的反应中,发生还原反应和发生氧化反应的物质,其质量比为( )
| A. | 1:1 | B. | 1:3 | C. | 1:2 | D. | 4:1 |
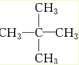 .
.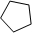 .
. A、B、C、D均为含苯环的有机物,且式量B>A>C.
A、B、C、D均为含苯环的有机物,且式量B>A>C. .
. .
. 、
、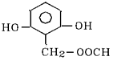 、
、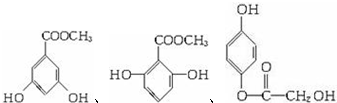 (其中的任意2种).
(其中的任意2种).