题目内容
5.在铜-锌(稀硫酸)原电池中,铜电极上发生还原反应(填“氧化”或“还原”),电极反应式为2H++2e-=H2↑;锌为负极(填“正”或“负”),电极反应式为Zn-2e-=Zn2+.分析 铜、锌、稀硫酸构成的原电池中,锌易失电子作负极,铜作正极,负极上失电子发生氧化反应,正极上得电子发生还原反应,据此分析解答.
解答 解:铜、锌、稀硫酸构成的原电池中,铜作正极,正极上氢离子得电子发生还原反应,电极反应式为2H++2e-=H2↑,铜电极上有氢气生成,所以看到的现象是铜片上有气泡产生,锌易失电子发生氧化反应而作负极,负极上电极反应式为 Zn-2e-=Zn2+,
故答案为:还原;2H++2e-=H2↑;负;Zn-2e-=Zn2+.
点评 本题考查了原电池原理,明确正负极上得失电子、反应类型、电极反应式的书写即可解答,难度不大.

练习册系列答案
相关题目
15.现有溴苯、乙醇、甲苯、己烯四种液体,只用一种试剂就可以将它们区别开,这种试剂是( )
| A. | 溴水 | B. | 食盐水 | C. | NaOH溶液 | D. | 盐酸 |
16.实验室可以用铁片与稀硫酸反应制取氢气,下列措施不能使氢气的生成速率增大的是( )
| A. | 加热 | |
| B. | 不用稀硫酸,改用质量分数为98%的浓硫酸 | |
| C. | 不用铁片改用镁条 | |
| D. | 不用铁片,改用铁粉 |
10.既可以用来鉴别乙烯和甲烷,又可用来除去甲烷中混有的乙烯的试剂或方法是( )
| A. | 溴水 | B. | 酸性高锰酸钾溶液 | ||
| C. | 在导管口处点燃 | D. | 一定条件下与氢气反应 |
17.下列关于有机反应的说法不正确的是( )
| A. | 乙醇可以发生连续氧化生成乙酸,从氧化还原角度来说在一定条件下乙醛可以发生歧化反应 | |
| B. | 2CH2=CHCl$\stackrel{催化剂}{→}$CH2=CH2+ClCH=CHCl此反应为取代反应 | |
| C. | 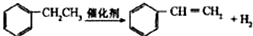 此反应为氧化反应 此反应为氧化反应 | |
| D. |  此反应为消去反应 此反应为消去反应 |
14.苯乙烯是一种重要的有机化工原料,其结构简式为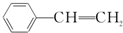 ,它一般不可能具有的性质是( )
,它一般不可能具有的性质是( )
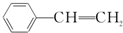 ,它一般不可能具有的性质是( )
,它一般不可能具有的性质是( )| A. | 易溶于水,不易溶于有机溶剂 | B. | 在空气中燃烧产生黑烟 | ||
| C. | 它能使溴的四氯化碳溶液褪色 | D. | 一定条件下可与氢气加成 |
4.中学化学教材中,常借助于图象的这一表现手段清晰地突出实验装置的要点、形象地阐述化学过程的原理.下列有关化学图象表现的内容正确的是( )
| A. | 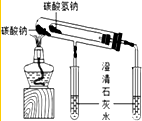 比较碳酸钠与碳酸氢钠的热稳定性 | B. |  称取NaOH | ||
| C. | 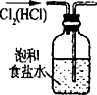 除去Cl2中HCl | D. | 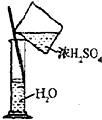 稀释浓H2SO4 |
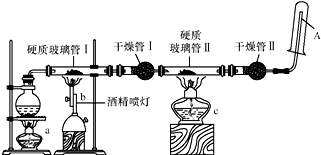 某研究性学习小组对教材中的铁与高温水蒸气反应的实验装置图做了如图所示的优化.通过观察硬质玻璃管Ⅱ和干燥管Ⅱ中的现象证明铁与水蒸气发生了反应,用试管收集产生的经干燥的气体,并靠近火焰点火,观察现象.请回答下列问题:
某研究性学习小组对教材中的铁与高温水蒸气反应的实验装置图做了如图所示的优化.通过观察硬质玻璃管Ⅱ和干燥管Ⅱ中的现象证明铁与水蒸气发生了反应,用试管收集产生的经干燥的气体,并靠近火焰点火,观察现象.请回答下列问题: