题目内容
7.已知铝也能和氢氧化钠溶液反应:2Al+2NaOH+2H2O→2NaAlO2+3H2↑,现有两份铝,一份与过量的氢氧化钠溶液反应,另一份与过量的盐酸反应,若要制取等质量的氢气,则两份铝的质量比为( )| A. | 1:1 | B. | 1:2 | C. | 2:3 | D. | 3:2 |
分析 铝与盐酸、氢氧化钠溶液的反应为氧化还原反应,Al在反应产物中都是+3价,根据电子守恒,生成等量的氢气消耗率的物质的量、质量一定相等.
解答 解:发生反应的方程式为:2Al+6HCl=2AlCl3+3H2↑、2Al+2NaOH+2H2O=2NaAlO2+3H2↑,两个反应都是氧化还原反应,根据电子守恒,当都生成相同的氢气时消耗的铝的质量应该相等,则质量比为1:1,
故选A
点评 本题考查氧化还原反应的简单计算,题目难度不大,明确发生反应的原理为解答关键,注意掌握电子守恒在氧化还原反应计算中的应用,试题侧重考查学生的分析能力及化学计算能力.

练习册系列答案
相关题目
11.120℃、101kPa时,两种气态烃的混合物2L完全燃烧,得到相同状况下3L CO2和3L水蒸气.这两种烃的可能组成是( )
| A. | CH4和C2H4 | B. | C2H6和C2H2 | C. | C3H8和C2H4 | D. | CH4和C2H2 |
18.下列离子方程式正确的是( )
| A. | Fe2O3溶于过量的氢碘酸中:Fe2O3+6H+=2Fe3++3H2O | |
| B. | 氯化铝溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓ | |
| C. | FeBr2溶液中加入过量的氯水:2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- | |
| D. | 铝和烧碱溶液:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
15.现有溴苯、乙醇、甲苯、己烯四种液体,只用一种试剂就可以将它们区别开,这种试剂是( )
| A. | 溴水 | B. | 食盐水 | C. | NaOH溶液 | D. | 盐酸 |
2.下列反应中属于吸热反应的是( )
| A. | 二氧化碳与赤热的炭反应生成一氧化碳 | |
| B. | 葡萄糖在人体内氧化分解 | |
| C. | 锌粒与稀硫酸反应制取氢气 | |
| D. | 氢氧化钠与盐酸反应 |
12.在相同条件下,把镁、铝、铁三种金属分别放入质量相等且足量的盐酸中,待反应完全后,三种溶液的质量相等,则投入的镁、铝、铁三种金属的质量关系是( )
| A. | Al>Mg>Fe | B. | Al=Mg=Fe | C. | Fe>Mg>Al | D. | Mg>Al>Fe |
16.实验室可以用铁片与稀硫酸反应制取氢气,下列措施不能使氢气的生成速率增大的是( )
| A. | 加热 | |
| B. | 不用稀硫酸,改用质量分数为98%的浓硫酸 | |
| C. | 不用铁片改用镁条 | |
| D. | 不用铁片,改用铁粉 |
17.下列关于有机反应的说法不正确的是( )
| A. | 乙醇可以发生连续氧化生成乙酸,从氧化还原角度来说在一定条件下乙醛可以发生歧化反应 | |
| B. | 2CH2=CHCl$\stackrel{催化剂}{→}$CH2=CH2+ClCH=CHCl此反应为取代反应 | |
| C. | 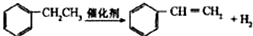 此反应为氧化反应 此反应为氧化反应 | |
| D. |  此反应为消去反应 此反应为消去反应 |