题目内容
4.在一定温度下,反应H2(g)+I2(g)?2HI(g)达到化学平衡状态的标志是( )| A. | 单位时间内生成n mol H2,同时就有n mol HI生成 | |
| B. | 单位时间内有n mol H2生成,同时就有n mol I2生成 | |
| C. | 容器内H2的含量不随时间的变化而变化 | |
| D. | 1个H-H键断裂的同时,有2个H-I键形成 |
分析 反应H2(g)+I2(g)?2HI(g)为可逆反应,无论是否达到平衡状态,都存在H2、I2、HI在容器中共存的特点,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不再变化,由此衍生的一些物理量不变,据此进行解答.
解答 解:A.单位时间内生成n mol H2,同时就有n mol HI生成,表示的是正逆反应,但不满足计量数关系,说明没有达到平衡状态,故A错误;
B.单位时间内有n mol H2生成,同时就有n mol I2生成,表示的都是逆反应速率,无法判断正逆反应速率是否相等,故B错误;
C.容器内H2的含量不随时间的变化而变化,说明正逆反应速率相等,该反应已经达到平衡状态,故C正确;
D.1个H-H键断裂的同时,有2个H-I键形成,表示的都是正反应速率,无法判断平衡状态,故D错误;
故选C.
点评 本题考查化学平衡状态的判断,题目难度不大,明确化学平衡状态的特征为解答关键,注意掌握化学平衡及其影响,试题有利于提高学生的灵活应用能力.

练习册系列答案
 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
14.下列装置或操作不能达到实验目的是( )
| A. |  装置关闭止水夹,往长颈漏斗加水,根据水位的变化情况可检查该装置的气密性 | |
| B. | 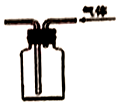 装置可用来收集NH3、H2等 | |
| C. |  装置可用来吸收极易溶于水的气体如NH3、HCl等 | |
| D. |  装置洗涤沉淀物时,向漏斗中加蒸馏水至浸没沉淀物,滤出溶液并重复操作2-3次 |
15.下列分离提纯方法正确的是( )
| A. | 除去乙醇中少量的水,加入新制的生石灰,过滤 | |
| B. | 提纯含有碘单质的食盐,常用升华法 | |
| C. | 除去乙酸乙酯中的乙酸,可加入NaOH溶液后分液 | |
| D. | 分离苯和酸性高锰酸钾溶液,蒸馏 |
12.按系统命名法有机物CH3CH2C(CH3)2CH(CH3)CH2CH3名称正确的是( )
| A. | 3,3-二甲基-4-乙基戊烷 | B. | 3,4-二甲基-4-乙基戊烷 | ||
| C. | 3,3,4-三甲基己烷 | D. | 3,4,4-三甲基己烷 |
19.下列有关“化学与生活”的叙述不正确的是( )
| A. | 点燃爆竹后,硫燃烧生成SO3 | |
| B. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| C. | 硫酸亚铁补血剂应与维生素C同服,是因为维生素C能防止Fe2+氧化 | |
| D. | 使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力减弱 |
9.某有机物其结构简式如图,关于该有机物的下列叙述正确的是( )


| A. | 能使酸性KMnO4溶液褪色 | |
| B. | 不能使溴水褪色 | |
| C. | 一定条件下,能和NaOH醇溶液反应 | |
| D. | 在加热和催化剂作用下,最多能和3 mol H2反应 |
16.根据下列事实所作的结论,正确的是( )
| 编号 | 事实 | 结论 |
| A | 甲、乙两种有机物具有相同相对分子质量和不同结构 | 甲和乙一定是同分异构体 |
| B | 质量相同的甲、乙两种有机物完全燃烧时产生质量相同的水 | 甲、乙两种分子中,各元素的原子个数比一定相同 |
| C | 在淀粉中加入稀H2SO4,水浴加热一段时间后取出部分水解液,滴加新制银氨溶液后再加热,无银镜出现 | 淀粉水解产物不具有还原性 |
| D | 不存在两种邻二甲苯 | 苯分子中碳碳键完全相同,而不是单双键交替结构 |
| A. | A | B. | B | C. | C | D. | D |
13.苹果酸的结构简式是 ,下列说法不正确的是( )
,下列说法不正确的是( )
 ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | 苹果酸能发生催化氧化反应 | |
| B. | 1 mol苹果酸可与3 mol NaOH发生中和反应 | |
| C. | 苹果酸能发生消去反应 | |
| D. | 苹果酸能发生缩聚反应 |
14.铝、铍(Be)及其化合物具有相似的化学性质,已知:BeCl2+Na2BeO2+2H2O═2NaCl+2Be(OH)2↓能完全进行,则下列推断正确的是( )
| A. | BeCl2溶液的pH<7,将其蒸干并灼烧后得到的残留物可能是BeCl2 | |
| B. | Be(OH)2既能溶于盐酸,又能溶于NaOH溶液 | |
| C. | Na2BeO2溶液的pH>7,将其蒸干并灼烧后得到的残留物为BeO | |
| D. | BeCl2水溶液的导电性强,故BeCl2是离子化合物 |