题目内容
7.25℃时,若10mL pH=a的盐酸与100mL pH=b的Ba(OH)2溶液恰好完全反应,则a+b的值为( )| A. | 14 | B. | 15 | C. | 13 | D. | 无法确定 |
分析 25℃时,若10mL pH=a的盐酸与100mL pH=b的Ba(OH)2溶液恰好完全反应,说明酸中n(H+)等于碱中n(OH-),据此计算a+b.
解答 解:酸中c(H+)=10-a mol/L,碱中c(OH-)=$\frac{1{0}^{-14}}{1{0}^{-b}}$mol/L=10 b-14 mol/L,若10mL pH=a的盐酸与100mL pH=b的Ba(OH)2溶液恰好完全反应,说明酸中n(H+)等于碱中n(OH-),所以0.01L×10-a mol/L=0.1L×10 b-14 mol/L,a+b=13,
故选C.
点评 本题考查pH值有关计算,侧重考查学生分析判断及计算能力,明确“酸中n(H+)与碱中n(OH-)的关系是解本题关键”,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
17.有关实验操作,下列说法中正确的是( )
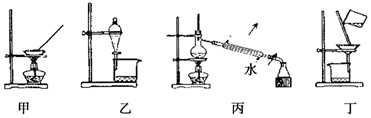

| A. | 甲装置可用于从氯化钠溶液中提取氯化钠 | |
| B. | 乙装置可用于分离溴单质与四氯化碳 | |
| C. | 丙装置可用于蒸馏,分离I2和水 | |
| D. | 丁装置可用于过滤,分离汽油和水的混合物 |
18.下列实验中,所选装置不合理的是( )
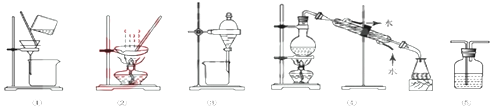

| A. | 分离Na2CO3溶液和CH3COOC2H5,选④ | B. | 粗盐提纯,选①和② | ||
| C. | 用FeC12溶液吸收C12,选⑤ | D. | 用CC14提取碘水中的碘,选③ |
15.下列叙述正确的是( )
| A. | Cu与过量的S混合加热,最终得到CuS | |
| B. | AlCl3、FeCl2、FeCl3均可通过化合反应制得 | |
| C. | 常温下,将27 g A1投入足量18.4 mol•L-1的硫酸中,产生1.5 mol H2 | |
| D. | 将CO2不断通入Ca(OH)2溶液中,最终得到白色沉淀 |
12.下列各物质属于电解质的是( )
①NaOH②BaSO4③Cu④蔗糖⑤CO2.
①NaOH②BaSO4③Cu④蔗糖⑤CO2.
| A. | ①② | B. | ①②⑤ | C. | ③④ | D. | ①③⑤ |
10.c(H+)相同的盐酸溶液和醋酸溶液分别与锌反应,若最后锌都己完全溶解,但放出的气体一样多,则下列判断正确的是( )
| A. | 整个反应阶段平均速率:醋酸>盐酸 | B. | 反应所需时间:醋酸>盐酸 | ||
| C. | 参加反应的锌质量:盐酸>醋酸 | D. | 开始,反应速率:盐酸>醋酸 |
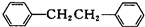 )是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
)是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为: