题目内容
10.下列装置所示的实验中,能达到实验目的是( )| A. | 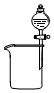 分离碘和酒精 | B. | 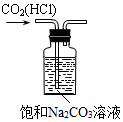 除去CO2中的HCl | C. | 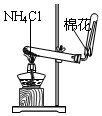 实验室制氨气 | D. | 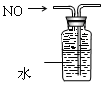 排水法收集NO |
分析 A.碘单质和酒精不分层,不能通过分液分离;
B.二氧化碳能够与碳酸钠溶液反应;
C.氯化铵分解生成的氨气和氯化氢反应;
D.NO不溶于水,可以用排水法收集.
解答 解:A.酒精与水相互溶解,二者不分层,无法通过分液分离,故A错误;
B.由于碳酸钠与二氧化碳反应,违反了除杂原则,应该用饱和碳酸氢钠溶液,故B错误;
C.氨气与HCl遇冷又会生成氯化铵,该方法无法制取氨气,故C错误;
D.一氧化氮气体不溶于水,图示通过图示装置用排水法收集NO,故D正确;
故选D.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及分液、物质分离与提纯、气体制备与收集等知识,明确常见化学实验基本操作方法为解答关键,试题有利于提高学生的化学实验能力.

练习册系列答案
相关题目
20.下列过程中△H小于零的是( )
| A. | Ba(OH)2与NH4Cl固体混合 | B. | 氯化铵分解得氨气 | ||
| C. | 碳酸钙分解得二氧化碳 | D. | 实验室制备氢气 |
1.X、Y、Z、W 为四种短周期主族元素,且原子序数依次增大.已知X原子的最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,Y原子的最层电子数是W原子最外层电子数的2倍,Z原子的最外层上只有一个电子.下列说法正确的是( )
| A. | 原子半径:r(Z)>r(W)>r(X)>r(Y) | |
| B. | Y与Z 两种元素只能形成一种化合物 | |
| C. | 最高价氧化物对应水化物的碱性:Z<W | |
| D. | X的简单气态氢化物的热稳定性比Y的强 |
5.硫酸铁铵[Fe2(SO4)3•(NH4)2SO4•6H2O]广泛用于生活用水的净化处理.制备硫酸铁铵的实验中,过滤出产品后,常温下另取母液(pH<1),向其中加入指定物质,反应后溶液中主要存在的一组离子正确的是( )
| A. | 加入过量NaOH溶液:Na+、NH4+、SO42-、OH- | |
| B. | 加入过量KI溶液:K+、Fe2+、NH4+、SO42-、I- | |
| C. | 加入过量BaCl2溶液:Ba2+、NH4+、Fe3+、SO42-、Cl- | |
| D. | 加入过量KSCN溶液:K+、NH4+、Fe3+、SO42-、SCN- |
2.设NA为阿伏加德罗常数的值.下列有关叙述正确的是( )
| A. | 常温常压下,5.6L甲烷与乙烯的混合气体中含氮原子数为NA | |
| B. | 72gCaO2固体中含离子总数为3NA | |
| C. | 向1LO.lmol/LKMnO4酸性溶液中通入足量SO2,转移电子效为0.5NA | |
| D. | 0.lmol氯气完全溶于水得1L氯水,溶液中ClO-数目是0.1NA |
19.下列有关实验装置进行的相应实验,能达到实验目的是( )
| A. | 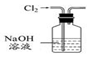 用图所示装置除去Cl2中含有的少量HCl | |
| B. | 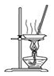 用图所示装置蒸干FeCl3饱和溶液制备FeCl3固体 | |
| C. | 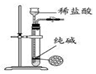 用图所示装置制取少量纯净的CO2气体 | |
| D. | 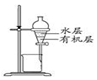 用图所示装置分离CCl4萃取碘水后已分层的有机层和水层 |
20.油酸跟油脂(相对分子质量884)在体内代谢时可发生如下反应:C57H104O6(s)+80O2(g)═57CO2(g)+52H2O(l)已知燃烧1kg该化合物释放出热量3.8×104kJ.油酸甘油酯的燃烧热△H为( )
| A. | -3.4×104kJ•mol-1 | B. | 3.4×104kJ•mol-1 | ||
| C. | -3.8×104kJ•mol-1 | D. | 3.8×104kJ•mol-1 |
 ,Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为1:1.
,Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为1:1.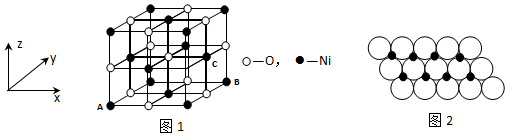
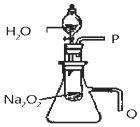 实验法是化学重要的研究物质性质的基本方法.某化学研究小组进行了如下实验,请回答问题.
实验法是化学重要的研究物质性质的基本方法.某化学研究小组进行了如下实验,请回答问题.