题目内容
下列有关实验的叙述中正确的是( )
| A、用烧杯给液态物质加热时,不用垫石棉垫 |
| B、加热蒸干AlCl3溶液得到Al2O3固体 |
| C、在用托盘天平称量固体药品时,药品放在右盘上 |
| D、如果未知溶液中滴加BaCl2溶液有白色沉淀生成,证明一定含有SO42-离子 |
考点:间接加热的仪器及使用方法,盐类水解的应用,硫酸根离子的检验,计量仪器及使用方法
专题:
分析:A.需要垫石棉网的是:烧杯、烧瓶、锥形瓶等;
B.加热促进AlCl3溶液水解;
C.托盘天平称量固体药品时,左物右码,并垫质量、大小相等的纸片;
D.在检验是否含有硫酸根离子时,如果对溶液成分没有限制,则需要可能存在的其他微粒如碳酸根离子、银离子等的干扰.
B.加热促进AlCl3溶液水解;
C.托盘天平称量固体药品时,左物右码,并垫质量、大小相等的纸片;
D.在检验是否含有硫酸根离子时,如果对溶液成分没有限制,则需要可能存在的其他微粒如碳酸根离子、银离子等的干扰.
解答:
解:A.烧杯、烧瓶不能直接加热,需垫石棉网,故A错误;
B.加热促进AlCl3溶液水解,生成Al(OH)3和HCl,HCl易挥发,蒸干得到Al2O3,故B正确;
C.称量时将药品放在左盘,砝码放在右盘,药品的质量等于砝码和游码的质量之和,并垫质量、大小相等的纸片,不能直接称量,潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,故C错误;
D.向该溶液滴加BaCl2溶液,当不加稀硝酸时,沉淀可能是由于Ba2+造成的BaCO3或者是BaSO4,也可能是由于Cl-生成的AgCl沉淀.由于后来又滴加了稀硝酸,沉淀不溶解,所以该沉淀可能是BaSO4或者是AgCl,故D错误.
故选B.
B.加热促进AlCl3溶液水解,生成Al(OH)3和HCl,HCl易挥发,蒸干得到Al2O3,故B正确;
C.称量时将药品放在左盘,砝码放在右盘,药品的质量等于砝码和游码的质量之和,并垫质量、大小相等的纸片,不能直接称量,潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,故C错误;
D.向该溶液滴加BaCl2溶液,当不加稀硝酸时,沉淀可能是由于Ba2+造成的BaCO3或者是BaSO4,也可能是由于Cl-生成的AgCl沉淀.由于后来又滴加了稀硝酸,沉淀不溶解,所以该沉淀可能是BaSO4或者是AgCl,故D错误.
故选B.
点评:本题考查化学实验基本操作,难度不大,注意掌握硫酸根离子的检验.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
在下列各溶液中,离子一定能大量共存的是( )
| A、室温下,pH=1的盐酸中:Na+、Fe3+、NO3-、SO42- |
| B、强碱性溶液中:K+、Mg2+、Cl-、SO42- |
| C、含有Ca2+的溶液中:Na+、K+、CO32-、Cl- |
| D、由水电离产生的c(H+)=1×10-13mol/L的溶液中:Na+、K+、SiO32-、Cl- |
 增塑剂(DEHP)的结构简式如图所示,下列有关增塑剂的说法不正确的是( )
增塑剂(DEHP)的结构简式如图所示,下列有关增塑剂的说法不正确的是( )| A、DEHP的分子式为C24H35O4 |
| B、DEHP在碱性条件下能水解 |
C、DEHP可由 和 和 在高温与催化剂条件下制得 在高温与催化剂条件下制得 |
| D、DEHP不能用作食品添加剂 |
在乙酸乙酯、乙醇、乙酸水溶液共存的化学平衡体系中加入含重氢的水,经过足够长的时间后,可以发现,除了水外,体系中含有重氢的化合物是( )
| A、只有乙醇 |
| B、只有乙酸 |
| C、乙酸乙酯、乙醇、乙酸 |
| D、只有乙醇和乙酸 |

 乙酸是实验室常用的化学药品之一.请回答下列问题:
乙酸是实验室常用的化学药品之一.请回答下列问题: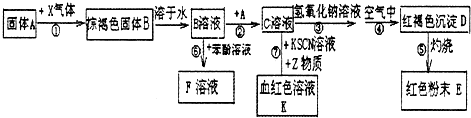
 钢铁等铁制品是应用最广泛的金属材料,铁元素的单质及其化合物在元素化合物世界始终扮演着重要角色.
钢铁等铁制品是应用最广泛的金属材料,铁元素的单质及其化合物在元素化合物世界始终扮演着重要角色.