题目内容
在乙酸乙酯、乙醇、乙酸水溶液共存的化学平衡体系中加入含重氢的水,经过足够长的时间后,可以发现,除了水外,体系中含有重氢的化合物是( )
| A、只有乙醇 |
| B、只有乙酸 |
| C、乙酸乙酯、乙醇、乙酸 |
| D、只有乙醇和乙酸 |
考点:酯的性质,化学反应的可逆性
专题:有机反应
分析:依据酯化反应的原理:酸去羟基,醇去氢;而酯化反应为可逆反应,酯化反应生成的H-OH中的羟基来自羧酸、氢原子来自醇,向体系中加入含重氢的水,经过足够长的时间后,重水中的-OD进入了羧酸,D原子进入乙醇,据此解答.
解答:
解:酯化反应的原理:酸去羟基,醇去氢;而酯化反应为可逆反应,酯化反应生成的H-OH中的羟基来自羧酸、氢原子来自醇,向体系中加入含重氢的水,经过足够长的时间后,重水中的-OD进入了羧酸,D原子进入乙醇,
所以最终含有重氢的化合物是乙酸乙酯和乙醇,
故选D.
所以最终含有重氢的化合物是乙酸乙酯和乙醇,
故选D.
点评:本题考查酯化反应、酯的水解反应产物,明确酯化反应的原理是解题关键,注意酯化反应是可逆反应,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
将a mol氮气和b mol氢气及c mol氨气混合充入一密闭容器中反应,在一定条件下到达平衡时,测知容器内氨气为x mol 这x的取值为( )
| A、c+2a | ||
B、
| ||
| C、0<x<c | ||
| D、c<x<c+2a |
下列有关实验的叙述中正确的是( )
| A、用烧杯给液态物质加热时,不用垫石棉垫 |
| B、加热蒸干AlCl3溶液得到Al2O3固体 |
| C、在用托盘天平称量固体药品时,药品放在右盘上 |
| D、如果未知溶液中滴加BaCl2溶液有白色沉淀生成,证明一定含有SO42-离子 |
荧光素(X)常用于钞票等防伪印刷,下列关于它的说法正确的是( )
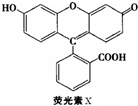

| A、荧光素的分子式为C20H14O5 |
| B、1molX最多能与9mol氢气反应 |
| C、1molX与足量的浓溴水反应,最多消耗4molBr2 |
| D、X能与甲醛发生缩聚反应 |
氨水中各离子和分子的浓度大小关系为( )
| A、c(NH4+)=c(OH-)=c(NH3?H2O) |
| B、c(NH4+)<c(OH-)<c(NH3?H2O) |
| C、c(NH4+)=c(OH-)<c(NH3?H2O) |
| D、c(NH4+)>c(OH-)>c(NH3?H2O) |
现向一含有Cu2+、Ca2+的混合溶液中滴入Na2CO3溶液,若首先生成CuCO3沉淀,据此可以得出的结论是( )
| A、Km(CuCO3)<Km(CaCO3) | ||||
| B、C[Cu2+]<c[Ca2+] | ||||
C、
| ||||
D、
|
在如图装置中,若通电一段时间后乙装置左侧电极增加,则下列说法中错误的是( )


| A、乙中左侧电极反应式:Cu2++2e-═Cu |
| B、电解过程中装置丙的pH无变化 |
| C、向甲中通入适量的HCI气体,可使溶液恢复到电解前的状态 |
| D、当甲装置中产生标准状况下4.48L气体时,Cu电极上质量增加43.2g |
把锌片投入盛有盐酸的敞口容器里,在下列因素中:①盐酸的浓度;②锌片的表面积;③溶液的温度;④氯离子的浓度;⑤溶液中加入少量CuSO4,对反应速率有影响的是( )
| A、①② | B、③④⑤ |
| C、①②③④ | D、①②③⑤ |
 可简写为
可简写为 .现有某化合物X的分子结构可表示为
.现有某化合物X的分子结构可表示为 .
.