题目内容
1. X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示.若X原子的最外层电子数是内层电子数的2倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如图所示.若X原子的最外层电子数是内层电子数的2倍,下列说法中正确的是( )| A. | X、Y对应的氧化物都是酸性氧化物 | |
| B. | 最高价氧化物对应水化物的酸性W比Z弱 | |
| C. | Z比Y更容易与氢气化合 | |
| D. | W、Z对应的最高价氧化物对应的水化物的相对分子质量相等 |
分析 X、Y、Z、W均为短周期元素,若X原子的最外层电子是内层电子数的2倍,则X原子有2个电子层,最外层电子数为4,所以X为C元素,根据X、Y、Z、W在周期表中相对位置可知,Y为N元素,Z为P元素,W为S元素,结合元素性质的递变规律分析解答.
解答 解:由以上分析可知X为C元素,Y为N元素,Z为P元素,W为S元素,
A.X、Y对应的氧化物如分别为CO、NO等,则为不成盐氧化物,故A错误;
B.非金属性S>P,则S的最高价氧化物对应水化物的酸性较强,故B错误;
C.非金属性N>P,N更容易与氢气化合,故C错误;
D.W、Z对应的最高价氧化物对应的水化物分别为硫酸、磷酸,相对分子质量都为98,故D正确.
故选D.
点评 本题考查位置结构性质关系应用,为高考常见题型和高频考点,侧重考查学生的分析能力,X是解答本题的突破口,明确短周期及元素在周期表中的位置来推断,注意基础知识的理解掌握.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
11.短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d是淡黄色粉末,m为元素Y的单质,通常为无色无味的气体.上述物质的转化关系如图所示.下列说法错误的是( )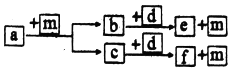

| A. | 简单离子半径:Z<Y | B. | 非金属性:X>Y | ||
| C. | 简单气态氢化物的热稳定性:Y>X | D. | W2Y2中含有共价键 |
12.下列有机物的命名错误的是( )
| A. | 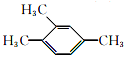 1,2,4-三甲苯 1,2,4-三甲苯 | B. |  2,2,4,4一四甲基戊烷 2,2,4,4一四甲基戊烷 | ||
| C. | 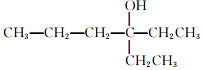 1,1-二乙基-1-丁醇 1,1-二乙基-1-丁醇 | D. |  1,3--溴丙烷 1,3--溴丙烷 |
9.下列实验操作正确且能达到相应实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 称取2.0g NaOH固体 | 先在左、右两托盘上各放一张滤纸,然后在有盘上添加2g砝码,左盘上添加NaOH固体 |
| B | 检验试液巾是否含有NH4+ | 取少量试液于试管巾,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
| C | 除去CO2中混有的杂质SO2 | 将混合气体通入盛有澄清石灰水的洗气瓶中 |
| D | 验证金属钠比铜活泼 | 将钠加入1.0mol•L-1的CuSO4溶液中 |
| A. | A | B. | B | C. | C | D. | D |
16.13C-NMR(核磁共振)可用于含碳化合物的结构分析.下列有关13C的说法不正确的是( )
| A. | 13C的质量数是13,核外有6个电子 | |
| B. | 13C 与12C是两种不同的核素 | |
| C. | 13C 与12C互为同位素 | |
| D. | 13C 与12C 的化学性质有很大的差别 |
6.甲、乙是周期表中同一周期的两种元素,甲在ⅡA族,乙在ⅣA族,那么甲、乙两元素的原子序数之差不可能是( )
| A. | 2 | B. | 12 | C. | 26 | D. | 11 |
13.下列关于热化学反应的描述中正确的是( )
| A. | NH4C1固体和Ba(OH)2晶体在常温下混合即可反应,是因为该反应是放热反应 | |
| B. | CO(g)的燃烧热是-283.0 KJ/mol,则 2CO2(g)═2CO(g)+O2(g)的反应热 为△H=+566.0 KJ/mol | |
| C. | 含1 mol Ba(OH)2的溶液和含1 mol H2SO4的溶液反应放出的热量是中和热 | |
| D. | 1 mol CH4燃烧生成水蒸气和二氧化碳所放出的热量是甲烷的燃烧热 |
5.下列物质中,不能使酸性KMnO4溶液褪色的物质是( )
①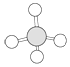 ②乙烯③CH3COOH④CH3CH2OH⑤CH2═CH-COOH ⑥
②乙烯③CH3COOH④CH3CH2OH⑤CH2═CH-COOH ⑥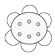
①
 ②乙烯③CH3COOH④CH3CH2OH⑤CH2═CH-COOH ⑥
②乙烯③CH3COOH④CH3CH2OH⑤CH2═CH-COOH ⑥
| A. | ①⑤ | B. | ①②④⑥ | C. | ①④ | D. | ①③⑥ |