题目内容
19.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )| A. | 25℃时,1L pH=13的Ba(OH)2溶液中含有OH一的数目为0.2NA | |
| B. | 取50mL 14.0moI.L-l浓硝酸与足量的铜片反应,生成气体分子的数目为0.35NA | |
| C. | 标准状况下,2.24L二氧化硫中含有的电子总数为3.2NA | |
| D. | 28gN2与28g C18O中含有的质子数均为14 |
分析 A.根据溶液的pH=13,求出c(H+)和c(OH-),然后根据n=CV求出氢氧根的个数;
B.浓硝酸随着反应的进行会逐渐变成稀硝酸,根据反应方程式Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O、3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O进行判断;
C.标准状况下2.24L二氧化硫的物质的量为0.1mol,二氧化硫分子中含有32个电子,0.1mol二氧化硫中含有3.2mol电子;
D.28g氮气的物质的量为1mol,含有14mol质子;28g C18O的物质的量需要1mol,含有质子数小于14mol.
解答 解:A.溶液的pH=13,可知c(H+)=10-13mol/L,故c(OH-)=0.1mol/L,氢氧根的物质的量n=CV=0.1mol/L×1L=0.1mol,故A错误;
B.铜与浓硝酸反应的方程式为:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,铜与稀硝酸反应的方程式为:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O,硝酸的物质的量为0.7mol,0.7mol浓硝酸完全反应生成0.35mol二氧化氮,0.7mol稀硝酸与铜反应生成0.175mol一氧化氮,所以0.7mol浓硝酸与足量铜反应生成的气体的物质的量小于0.35mol,生成的气体分子数小于0.35NA,故B错误;
C.标况下2.24L二氧化硫的物质的量为:$\frac{2.24L}{22.4L/mol}$=0.1mol,0.1mol二氧化硫中含有3.2mol电子,含有的电子总数为3.2NA,故C正确;
D.N2与C18O分子中都含有14个电子,而二者的摩尔质量不同,根据n=$\frac{m}{M}$可知,等质量的二者含有的质子数不同,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的综合应用,题目难度中等,以阿伏伽德罗常数为载体考查如下知识点有:①考查22.4L/mol的正确使用;②考查在氧化还原反应中得失电子数的计算;③正确表示一定物质的量的某物质微粒所含某种微粒的个数;④考查在标准状况下一定体积的气体分子所含的分子数和原子数.

| A. | SiO2 | B. | HCl | C. | FeCl2 | D. | NO |
(1)在高温下一氧化碳可将二氧化硫还原为单质硫.
乙知:C(s)+O2(g)=CO2(g)△H1=-393.5kJ/mol
CO2(g)+C(s)=2CO(g)△H2=172.5kJ/mol
S(s)+O2(g)=SO2(g)△H3=-296.0kJ/mol
则CO还原SO2生成CO2(g)和S(s)的热化学方程为2CO(g)+SO2(g)=S(s)+2CO2(g);△H3=-270 kJ•mol-1.
(2)工业上一般采用CO与H2在一定条件下反应合成甲醇,反应为:CO(g)+2H2(g)?CH3OH(g).在不同温度下的化学平衡常数(K)如表:
| 温度 | 250 | 300 | 350 |
| K | 2.041 | 0.250 | 0.012 |
②在恒容条件下,要提高CO(g)的转化率,呵以采取的措施有DE(填字母序号).
A.升高温度 B.加入催化剂 C.增加CO(g)的浓度D.充入H2(g)加压 E.分离出甲醇 F.充入稀有气体加压
③实际生产过程中,合成气要进行循环,其目的是提高原料利用率.
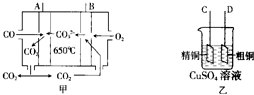
(3)如图图甲是一碳酸盐燃料电池,它以CO为燃料,一定比例的Li2CO3和Na2CO3熔融混合物为电解质;图乙是粗铜精炼的装置图,现用燃料电池为电源进行粗铜的精炼实验.
请问答下列问题:
①A极的电极反应式为CO-2e-+CO32-=2CO2.
②进行粗铜精炼实验时,B极应该与D极(填“C”或“D”)相连.
③当消耗2.24L(标准状况下)CO时,粗铜电极理论上减少铜的质量小于(填“大于”“等于”或“小于”)6.4克.
| 1 | 2 | 3 | 4 | 5 | 6 | … |
| CH4 | C2H6 | C5H12 | C8H18 | … | … | … |
| A. | C26H54 | B. | C17H36 | C. | C80H162 | D. | C106H214 |
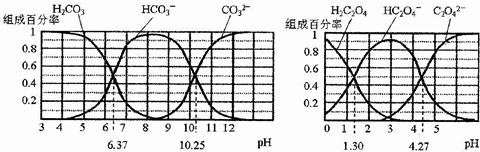
| A. | 在pH为6.37及10.25时,溶液中c(H2CO3)=c(HCO3-)=c(CO32-) | |
| B. | 反应HCO3-+H2O?H2CO3+OH-的平衡常数为10-10.25 | |
| C. | 0.1mol•L-1NaHC2O4溶液中c(HC2O4-)+c(H2C2O4)=0.1mol•L-1 | |
| D. | 往Na2CO3溶液中加入少量草酸溶液,发生反应:CO32-+H2C2O4=HCO3-+HC2O4- |
| A. | 参加反应所需NaOH与氯气的物质的量之比一定为2:1 | |
| B. | 反应体系中n(NaCl):n(NaClO):n(NaC1O3)(物质的量之比)可能为11:1:2 | |
| C. | 若反应有amol氯气参加反应,则amol<转移电子数<$\frac{5a}{3}$mol | |
| D. | 反应中NaC1O和NaClO3为氧化产物,且物质的量之比一定为l:1 |

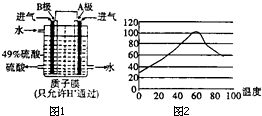
| A. | 上述过程中,NOX只被CO还原 | |
| B. | 安装该净化器的汽车使用含铅汽油不会造成污染 | |
| C. | 产生22.4L氮气(标准状况)时,转移4xmole- | |
| D. | Pt-Rh催化剂可提高尾气平衡转化率 |
 我国黄铁矿(主要成分:FeS2、SiO2)储量丰富,目前主要利用黄铁矿资源生产硫酸等无机化工产品.
我国黄铁矿(主要成分:FeS2、SiO2)储量丰富,目前主要利用黄铁矿资源生产硫酸等无机化工产品. ①烧渣用稀硫酸浸取时有单质硫生成,生成单质硫的一步化学反应方程式为H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4;
①烧渣用稀硫酸浸取时有单质硫生成,生成单质硫的一步化学反应方程式为H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4;