题目内容
14.下列各组物质中,所含分子数相同的是( )| A. | 5g H2 和 5g O2 | B. | 标况下 5.6L N2和 22g CO2 | ||
| C. | 32 g SO2和0.5molH2 | D. | 44.8 L CO和2NA个O3分子 |
分析 所含分子数相等,说明两种物质的物质的量相等,根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$计算其物质的量来判断即可.
解答 解:所含分子数相等,说明两种物质的物质的量相等,
A.根据n=$\frac{m}{M}$知,两种气体的质量相等但摩尔质量不等,所以其物质的量不等,所以分子数不等,故A错误;
B.标况下氮气物质的量=$\frac{V}{{V}_{m}}$=$\frac{5.6L}{22.4L/mol}$=0.25mol,22g CO2物质的量0.5mol,所以二者分子数不相等,故B错误;
C.32g二氧化硫物质的量=$\frac{32g}{64g/mol}$=0.5mol,所以二者分子数相等,故C正确;
D.标况下,44.8 二氧化碳物质的量为2mol,2NA个O3分子物质的量为2mol,而状况不知,故D错误;
故选C.
点评 本题考查物质的量的计算,侧重考查分析计算能力,明确物质的量公式中各个物理量的关系即可解答,注意气体摩尔体积适用范围及适用条件,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列离子组能以较大浓度共存的是( )
| A. | 含有0.1mol•L-1Fe3+的溶液中:K+、Mg2+、I-、NO3- | |
| B. | 使酚酞试液变红的溶液:Na+、Cl-、SO42-、CO32- | |
| C. | 含有0.1mol•L-1Ca2+的溶液中:Na+、K+、CO32-、Cl- | |
| D. | 碳酸氢钠溶液:K+、SO42-、Cl-、H+ |
5.用3g块状大理石与30mL 3mol•L-1盐酸反应制取CO2气体,若要增大反应速率,可采取的措施是( )
①再加入30mL 3mol•L-1盐酸 ②改用30mL 6mol•L-1盐酸 ③改用3g粉末状大理石.
①再加入30mL 3mol•L-1盐酸 ②改用30mL 6mol•L-1盐酸 ③改用3g粉末状大理石.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
2.下列物质中,不能由两种单质直接化合得到的是( )
| A. | HCl | B. | Na2O2 | C. | MgO | D. | FeCl2 |
9.某同学用托盘天平称量镁粉25.6g(1g以下用游码),他把镁粉放在左盘,当天平平衡时,所称取的镁粉的实际质量是( )
| A. | 25.6g | B. | 24.4g | C. | 24.6g | D. | 262g |
19.下列叙述错误的是( )
①摩尔是国际单位制中七个基本物理量之一;②1mol任何物质都含有约6.02×1023个原子;③物质的量浓度为0.1mol/L的AlCl3溶液中,Cl-的个数是0.3NA;④氢原子的摩尔质量是1g;⑤HCl的摩尔质量就是1mol HCl分子的质量;⑥1mol SO2的体积是22.4L.
①摩尔是国际单位制中七个基本物理量之一;②1mol任何物质都含有约6.02×1023个原子;③物质的量浓度为0.1mol/L的AlCl3溶液中,Cl-的个数是0.3NA;④氢原子的摩尔质量是1g;⑤HCl的摩尔质量就是1mol HCl分子的质量;⑥1mol SO2的体积是22.4L.
| A. | ①②⑤ | B. | ②③④ | C. | ②④⑤⑥ | D. | 全部 |
6.在容积可变的密闭容器中存在如下反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,下列分析中正确的是( )
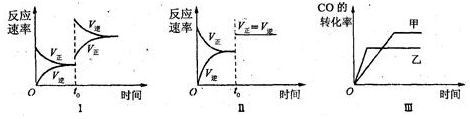

| A. | 图Ⅱ研究的只是t0时使用催化剂对反应速率的影响 | |
| B. | 图Ⅰ研究的是t0时缩小容器体积对反应速率的影响 | |
| C. | 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 | |
| D. | 图Ⅲ研究的是催化剂对化学平衡的影响,且甲使用了催化剂 |
3.下列事实不能用勒夏特列原理解释的是( )
| A. | 由H2(g)、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 | |
| B. | 高压比常压有利于由SO2和氧气合成SO3的反应 | |
| C. | 红棕色的NO2,加压后颜色先变深后变浅 | |
| D. | 黄绿色的氯水光照后颜色变浅 |
4.高铁酸钾(K2FeO4)是一种集氧化,吸附,絮凝于一体的新型多功能水处理剂,高铁酸盐热 稳定性差.制备方法有湿法、干法两种,其原理如下表所示:
湿法的生产工艺如图:

回答下列问题:
(1)K2FeO4 中 Fe 的化合价+6;实验室干法制备中选用的仪器是 B
A.蒸发皿 B.铁坩埚 C.氧化铝坩埚 D.陶瓷坩埚
(2)在温度较高时 KOH 与 Cl2 反应生成的是 KClO3,写出在温度较高时 KOH 与 Cl2反应的化学方程式6KOH+3Cl2$\frac{\underline{\;高温\;}}{\;}$KClO3+5KCl+3H2O
(3)在溶液 I 中加入 KOH 固体的目的是 BD
A.使 KClO3 转化为 KClO
B.为下一步反应提供碱性的环境
C.KOH 固体溶解放热,有利于提高反应速率
D.与溶液 I 中过量的 Cl2 继续反应,生成更多的 KClO
(4)向次氯酸钾强碱浓溶液中加入 90%的 Fe(NO3)3,发生反应的离子方程式为:
①Fe3++3OH+═Fe(OH)3
②3ClO-+10OH-+2Fe3+=2FeO42-+3Cl-+5H2O.
(5)用异丙醇代替蒸馏水洗涤湿产品,除能洗去杂质外,其优点有减少K2FeO4晶体洗涤时产品的损失且产品易干燥.
(6)如何判断 K2FeO4 晶体已经洗涤干净取少量最后一次的洗涤液于试管中,加入硝酸银溶液,无白色沉淀则已被洗净.
(7)高铁酸钾(K2FeO4)作为水处理剂的优点之一是能除去悬浮杂质,配平该反应的离子方程式:
4FeO42-+10H2O═4Fe(OH)3(胶体)+3O2↑+8OH-.
| 干法 | Fe2O3、KNO3、KOH 混合加热共熔生成紫红色 K2FeO4 和 KNO2 等产物 |
| 湿法 | 强碱性介质中,Fe(NO3)3和 KClO 反应生成紫红色 K2FeO4溶液 |

回答下列问题:
(1)K2FeO4 中 Fe 的化合价+6;实验室干法制备中选用的仪器是 B
A.蒸发皿 B.铁坩埚 C.氧化铝坩埚 D.陶瓷坩埚
(2)在温度较高时 KOH 与 Cl2 反应生成的是 KClO3,写出在温度较高时 KOH 与 Cl2反应的化学方程式6KOH+3Cl2$\frac{\underline{\;高温\;}}{\;}$KClO3+5KCl+3H2O
(3)在溶液 I 中加入 KOH 固体的目的是 BD
A.使 KClO3 转化为 KClO
B.为下一步反应提供碱性的环境
C.KOH 固体溶解放热,有利于提高反应速率
D.与溶液 I 中过量的 Cl2 继续反应,生成更多的 KClO
(4)向次氯酸钾强碱浓溶液中加入 90%的 Fe(NO3)3,发生反应的离子方程式为:
①Fe3++3OH+═Fe(OH)3
②3ClO-+10OH-+2Fe3+=2FeO42-+3Cl-+5H2O.
(5)用异丙醇代替蒸馏水洗涤湿产品,除能洗去杂质外,其优点有减少K2FeO4晶体洗涤时产品的损失且产品易干燥.
(6)如何判断 K2FeO4 晶体已经洗涤干净取少量最后一次的洗涤液于试管中,加入硝酸银溶液,无白色沉淀则已被洗净.
(7)高铁酸钾(K2FeO4)作为水处理剂的优点之一是能除去悬浮杂质,配平该反应的离子方程式:
4FeO42-+10H2O═4Fe(OH)3(胶体)+3O2↑+8OH-.