��Ŀ����
����Ŀ������������ȼ�ϵ��������������(Westinghouse)��˾���ƿ����ģ����Թ��������һ������Ϊ����ʣ����ֹ��������ڸ���������������(O2-)�����ͨ�����õ�صĹ���ԭ����ͼ��ʾ�����ж�缫a��b��������缫��Ӧ�������ж���ȷ����
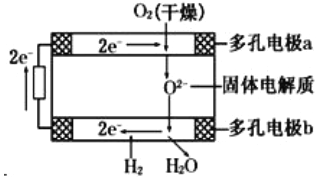
A����O2�ŵ��a��Ϊ��صĸ���
B��O2-�����ص�����
C��b����Ӧ�ĵ缫��ӦΪ2H2- 4e-+2O2-=2H2O
D��a����Ӧ�ĵ缫��ӦΪO2+2H2O+4e-=4OH-
���𰸡�C
��������
���������A����ȼ�ϵ���У���O2�ŵ��a��Ϊԭ��ص�������A����B��ԭ�����������������B����C��b�������ŵ磬�Ǹ�������Ӧ�ĵ缫��ӦΪ2H2-4e-+2O2-��2H2O��C��ȷ��D��a���������ŵ磬��Ӧ�ĵ缫��ӦΪ��O2+4e-��2O2-��D��������ѡC��

��ϰ��ϵ�д�
 ѧ���쳵��������������������ϵ�д�
ѧ���쳵��������������������ϵ�д�
�����Ŀ