题目内容
已知反应3S+6KOH(浓)
2K2S+K2SO3+3H2O,则反应中氧化剂和还原剂的质量比是( )
| ||
| A、3:1 | B、1:3 |
| C、2:1 | D、1:2 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:化合价升高所在的反应物是还原剂,化合价降低元素所在的反应物是氧化剂,据此分析.
解答:
解:反应3S+6KOH(浓)═2K2S+K2SO3+3H2O中,硫元素化合价既升高又降低,所以硫单质既是氧化剂又是还原剂,在参与反应的3mol硫中,其中1mol做还原剂,2mol做氧化剂,所以反应中氧化剂和还原剂的物质的量之比是2:1,质量比也是2:1.
故选C.
故选C.
点评:本题考查学生氧化还原反应的基本概念,侧重于氧化还原反应的概念的考查,题目难度不大.

练习册系列答案
相关题目
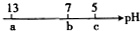 已知二元含氧酸H2X易溶于水,向1.0mol?L-1 的酸式盐NaHX中滴入几滴石蕊试剂,溶液变红.下列说法错误的是( )
已知二元含氧酸H2X易溶于水,向1.0mol?L-1 的酸式盐NaHX中滴入几滴石蕊试剂,溶液变红.下列说法错误的是( )| A、NaHX溶液呈酸性 |
| B、若上述溶液中检测不到HX-,则NaHX溶于水时的电离方程式为:NaHX=Na++H++X- |
| C、若上述溶液中检测不到H2X,但能检测到HX-,则NaHX溶于水时,水的电离程度增大 |
| D、若上述溶液中能检测到H2X,则此时溶液中c(X2-)>c(H2X) |
对已经达到化学平衡的下列反应:2X(g)+Y(g)?2Z(g),减小压强时( )
| A、逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B、逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C、正、逆反应速率都减小,平衡向逆反应方向移动 |
| D、正、逆反应速率都增大,平衡向正反应方向移动 |
误服重金属盐会引起中毒,下列措施不能达到解毒作用的是( )
| A、服用大量鸡蛋清 |
| B、服用豆浆 |
| C、喝大量牛奶 |
| D、喝食盐水 |
下列实验合理的是( )
A、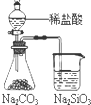 证明非金性Cl>C>Si |
B、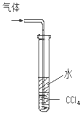 吸收氨气并防止倒吸 |
C、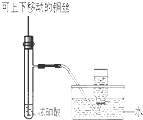 制备并收集少量NO2气体 |
D、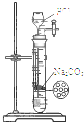 制备CO2 |
下列说法中正确的是( )
| A、由分子构成的物质中一定含有共价键 |
| B、正四面体结构的分子中键角一定是109028’ |
| C、形成共价键的元素不一定是非金属元素 |
| D、CO2 和SiO2都是直线型分子 |
某氯化镁溶液的密度为1.6g?cm-3,其中镁离子的质量分数为5%,300mL该溶液中Cl-离子的物质的量约等于( )
| A、0.37 mol |
| B、0.63mol |
| C、2 mol |
| D、1.5mol |
下列分散系能产生丁达尔效应的是( )
| A、氨气溶于水形成的氨水 |
| B、胆矾溶于水配制的硫酸铜溶液 |
| C、过滤浊液所得澄清石灰水 |
| D、分散在酒精中的氯化钠胶体 |
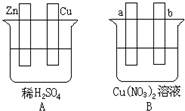 对如图中两极加以必要的连接并填空:
对如图中两极加以必要的连接并填空: