题目内容
下列有关实验操作、现象和解释或结论都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| C | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸 | 有气泡产生 | 不能说明常温下Kap(BaCO3)与Kap(BaSO4)的大小关系 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.过量的Fe粉中加入稀HNO3,生成硝酸亚铁;
B.AgI沉淀中滴入稀KCl溶液,若生成白色沉淀,则Qc(AgCl)>Ksp(AgCl);
C.饱和Na2CO3溶液中加少量BaSO4粉末,沉淀中加盐酸生成气体,则有碳酸钡,即Qc(BaCO3)>Ksp(BaCO3);
D.显碱性的溶液可使红色石蕊试纸变蓝.
B.AgI沉淀中滴入稀KCl溶液,若生成白色沉淀,则Qc(AgCl)>Ksp(AgCl);
C.饱和Na2CO3溶液中加少量BaSO4粉末,沉淀中加盐酸生成气体,则有碳酸钡,即Qc(BaCO3)>Ksp(BaCO3);
D.显碱性的溶液可使红色石蕊试纸变蓝.
解答:
解:A.过量的Fe粉中加入稀HNO3,生成硝酸亚铁,则滴入KSCN溶液无现象,故A错误;
B.AgI沉淀中滴入稀KCl溶液,若生成白色沉淀,则Qc(AgCl)>Ksp(AgCl),不能比较Ksp,且结论错误,故B错误;
C.饱和Na2CO3溶液中加少量BaSO4粉末,沉淀中加盐酸生成气体,则有碳酸钡,即Qc(BaCO3)>Ksp(BaCO3),发生沉淀的生成,而不是沉淀的转化,则不能说明常温下Kap(BaCO3)与Kap(BaSO4)的大小关系,故C正确;
D.显碱性的溶液可使红色石蕊试纸变蓝,则玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝,说明浓氨水呈碱性,故D正确;
故选CD.
B.AgI沉淀中滴入稀KCl溶液,若生成白色沉淀,则Qc(AgCl)>Ksp(AgCl),不能比较Ksp,且结论错误,故B错误;
C.饱和Na2CO3溶液中加少量BaSO4粉末,沉淀中加盐酸生成气体,则有碳酸钡,即Qc(BaCO3)>Ksp(BaCO3),发生沉淀的生成,而不是沉淀的转化,则不能说明常温下Kap(BaCO3)与Kap(BaSO4)的大小关系,故C正确;
D.显碱性的溶液可使红色石蕊试纸变蓝,则玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝,说明浓氨水呈碱性,故D正确;
故选CD.
点评:本题考查化学实验方案的评价,为高频考点,涉及氧化还原反应、沉淀的生成和转化、氨水的性质等,把握化学反应原理为解答的关键,选项BC为解答的难点,注意区分沉淀生成及转化及实验的评价性分析,题目难度不大.

练习册系列答案
 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案
相关题目
下列装置或操作合理的是( )
A、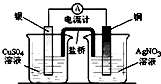 装置可将化学能转化为电能 |
B、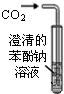 装置可用于比较碳酸、苯酚酸性的强弱 |
C、 装置可用来进行浓硫酸的稀释 |
D、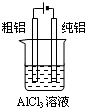 装置可用于电解精炼铝 |
不能鉴别乙酸溶液、乙醇溶液的试剂是( )
| A、氢氧化钠溶液 |
| B、氢氧化铜悬浊液 |
| C、石蕊试液 |
| D、碳酸钠溶液 |
己烯雌酚是一种激素类药物,结构如图所示,下列有关叙述中正确的是( )


| A、该分子对称性好,所以没有立体异构 |
| B、该分子中有2个H,2个O,6个C共直线 |
| C、分子中有7个碳碳双键,可以与氢气1:7加成 |
| D、该有机物分子中,最多可能有18个碳原子共平面 |
某学生将一小块钠投入滴有酚酞的水中,此实验能证明钠下面4点性质中的( )
①钠比水轻
②钠的熔点较低
③钠与水反应在时要放出热量
④钠与水反应后溶液呈碱性.
①钠比水轻
②钠的熔点较低
③钠与水反应在时要放出热量
④钠与水反应后溶液呈碱性.
| A、①④ | B、①②④ |
| C、①③④ | D、①②③④ |
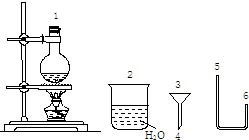 欲配制500mL0.2mol/LNa2CO3溶液,回答下列问题:
欲配制500mL0.2mol/LNa2CO3溶液,回答下列问题: