题目内容
11.有一种碘和氧的化合物可以称为碘酸碘,其中碘元素呈+3、+5两种价态,这种化学式和应当具有的性质为( )| A. | I2O4 强氧化性 | B. | I3O5 强还原性 | C. | I4O9 强氧化性 | D. | I4O7 强还原性 |
分析 碘酸碘的化学式一定为Im(IO3)n形式,其中碘酸根为-1价(类似于氯酸根),碘酸根中I为+5价,则前面的I为+3价,+5价碘具有强氧化性,以此解答该题.
解答 解:因碘酸碘的化学式一定为Im(IO3)n形式,其中碘酸根为-1价(类似于氯酸根),碘酸根中I的化合价为+5价,所以前面的I的化合价为+3价,所以碘酸碘的化学式为:I(IO3)3,即 I4O9,与碘酸钾性质相似,具有强氧化性,故选C.
点评 本题主要考查化合价的规律和原则,为高频考点,侧重考查学生的分析能力,同时还考查常见元素及原子团的化合价,难度中等,解题应抓住题目信息.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.网络神曲“化学是你,化学是我”揭示了化学与生活的密切关系.下列有关说法中正确的是( )
| A. | 青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是铝合金 | |
| B. | 碳酸钠俗名纯碱,也叫苏打,可用于清洗厨房用具的油污 | |
| C. | 钢铁生锈、沙里淘金、蒸馏法制取纯净水都涉及了化学变化 | |
| D. | 工业酒精既可以用作燃料制“乙醇汽油”,又可以勾兑成白酒饮用 |
2.氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:aHClO3=bO2↑+cCl2↑+dHClO4+eH2O.下列有关说法不正确的是( )
| A. | 由电子转移守恒和氯元素守恒可推出2b+a=6c | |
| B. | 若氯酸分解所得混合气体,在相同状态下密度是氢气的25.75信,则反应方程式可表示为:5HClO3=O2↑+Cl2↑+3HClO4+H2O | |
| C. | 由非金属性Cl>S,可推知酸性HClO4>H2SO4 | |
| D. | 若化学计量数a=3,b=2,则该反应转移电子数为10e- |
19.下列离子方程式中书写正确的是( )
| A. | NaHSO4在水溶液的电离方程式 NaHSO4?Na++H++SO42- | |
| B. | 氯化铵在氘水中的水解离子方程式 NH4++D2O?NH3•HDO+D+ | |
| C. | NaHS在水中的水解离子方程式 HS-+H2O?S2-+H3O+ | |
| D. | 碳酸钾固体在水中的水解离子方程式CO32-+2H2O?2OH-+H2CO3 |
6.用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 标准状况下,22.4L乙醇完全燃烧后生成CO2的分子数为2NA | |
| B. | 56g的铁发生氧化还原反应,一定失去3NA个电子 | |
| C. | 标准状况下,22.4L氧气和二氧化碳混合气体中所含氧原子数为2NA | |
| D. | 0.1mol/L稀硫酸中含有SO42-离子数为0.1NA |
15.下列有关化学用语正确的是( )
| A. | 二氧化碳的结构式:O-C-O | |
| B. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| C. | F原子结构示意图: | |
| D. | N2的电子式: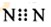 |
2.下列关于物质及其用途的关联中不正确的是( )
| A. | 乙醇-燃料 | B. | 蛋白质-生产葡萄糖 | ||
| C. | 淀粉-酿酒 | D. | 油脂-制造肥皂 |
18.以乙醇为基本有机原料自选其他无机试剂,不能合成的物质有( )
| A. | 乙醛 | B. | 乙酸 | C. | 甲烷 | D. | 丙酮 |