题目内容
污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题.某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略).
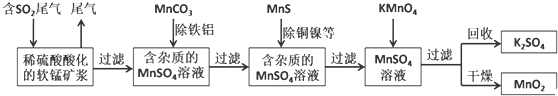
请回答下列问题:
(1)上述流程中多次涉及到过滤操作,实验室进行过滤操作时需要用到的硅酸盐仪器有玻璃棒、 、 ;其中玻璃棒的作用是 .
(2)用MnCO3能除去溶液中的Al3+和Fe3+,其原理是 .
(3)已知Ksp(CuS)=8.4×10-45,Ksp(NiS)=1.4×10-24;在除铜镍的过程中,当Ni2+恰好完全沉淀 (此时溶液中c(Ni2+)=1.0×10-5mol/L),溶液中Cu2+的浓度是 mol/L.
(4)工业上采用电解K2MnO4水溶液的方法来生产KMnO4,其中隋性电极作阳极,铁作阴极,请写出阳极的电极反应式 .
(5)下列各组试剂中,能准确测定一定体积燃煤尾气中SO2含量的是 .(填编号)
a.NaOH溶液、酚酞试液b.稀H2SO4酸化的KMnO4溶液c.碘水、淀粉溶液d.氨水、酚酞试液
(6)除杂后得到的MnSO4溶液可以通过 (填操作名称)制得硫酸锰晶体(MnSO4?H2O,相对分子质量为169).已知废气中SO2浓度为8.4g/m3,软锰矿浆对SO2的吸收率可达90%,则处理1000m3燃煤尾气,可得到硫酸锰晶体质量为 kg(结果保留3位有效数字).

请回答下列问题:
(1)上述流程中多次涉及到过滤操作,实验室进行过滤操作时需要用到的硅酸盐仪器有玻璃棒、
(2)用MnCO3能除去溶液中的Al3+和Fe3+,其原理是
(3)已知Ksp(CuS)=8.4×10-45,Ksp(NiS)=1.4×10-24;在除铜镍的过程中,当Ni2+恰好完全沉淀 (此时溶液中c(Ni2+)=1.0×10-5mol/L),溶液中Cu2+的浓度是
(4)工业上采用电解K2MnO4水溶液的方法来生产KMnO4,其中隋性电极作阳极,铁作阴极,请写出阳极的电极反应式
(5)下列各组试剂中,能准确测定一定体积燃煤尾气中SO2含量的是
a.NaOH溶液、酚酞试液b.稀H2SO4酸化的KMnO4溶液c.碘水、淀粉溶液d.氨水、酚酞试液
(6)除杂后得到的MnSO4溶液可以通过
考点:物质分离和提纯的方法和基本操作综合应用,物质的分离、提纯的基本方法选择与应用
专题:
分析:由流程可知,二氧化硫能与二氧化锰反应生成硫酸锰,用MnCO3能除去溶液中Al3+和Fe3+,MnS将铜、镍离子还原为单质,高锰酸钾能与硫酸锰反应生成二氧化锰,通过过滤获得二氧化锰,
(1)过滤需要漏斗、烧杯、玻璃棒等,玻璃棒起引流作用;
(2)从消耗溶液中的酸,促进Al3+和Fe3+水解角度分析;
(3)当Ni2+恰好完全沉淀 (此时溶液中c(Ni2+)=1.0×10-5mol/L),c(S2-)=
,结合Ksp(CuS)计算溶液中Cu2+的浓度;
(4)隋性电极作阳极,铁作阴极,则阳极上失去电子发生氧化反应;
(5)准确测定一定体积燃煤尾气中SO2含量,利用其还原性及明显的反应现象分析;
(6)由溶液得到晶体,应浓缩、结晶;结合硫原子守恒可知,被吸收的SO2的物质的量等于硫酸锰晶体的物质的量.
(1)过滤需要漏斗、烧杯、玻璃棒等,玻璃棒起引流作用;
(2)从消耗溶液中的酸,促进Al3+和Fe3+水解角度分析;
(3)当Ni2+恰好完全沉淀 (此时溶液中c(Ni2+)=1.0×10-5mol/L),c(S2-)=
| Ksp(NiS) |
| c(Ni2+) |
(4)隋性电极作阳极,铁作阴极,则阳极上失去电子发生氧化反应;
(5)准确测定一定体积燃煤尾气中SO2含量,利用其还原性及明显的反应现象分析;
(6)由溶液得到晶体,应浓缩、结晶;结合硫原子守恒可知,被吸收的SO2的物质的量等于硫酸锰晶体的物质的量.
解答:
解:由流程可知,二氧化硫能与二氧化锰反应生成硫酸锰,用MnCO3能除去溶液中Al3+和Fe3+,MnS将铜、镍离子还原为单质,高锰酸钾能与硫酸锰反应生成二氧化锰,通过过滤获得二氧化锰,
(1)过滤需要漏斗、烧杯、玻璃棒等,过滤中玻璃棒的作用为引流,防止液体溅出,故答案为:烧杯;漏斗;引流,防止液体溅出;
(2)由于碳酸锰能消耗溶液中的酸,降低溶液的酸性,从而促进Al3+和Fe3+水解生成氢氧化物沉淀,
故答案为:消耗溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀;
(3)当Ni2+恰好完全沉淀 (此时溶液中c(Ni2+)=1.0×10-5mol/L),c(S2-)=
=
=1.4×10-19,由Ksp(CuS)可知溶液中Cu2+的浓度为
=6.0×10-26mol/L,故答案为:6.0×10-26;
(4)隋性电极作阳极,铁作阴极,则阳极上失去电子发生氧化反应,则阳极反应为MnO42--e-═MnO4-,故答案为:MnO42--e-═MnO4-;
(5)准确测定一定体积燃煤尾气中SO2含量,二氧化硫与氨水、NaOH反应不易控制,且加指示剂现象观察的滴定终点与反应终点误差大,而b、c中利用还原性及高锰酸钾褪色、淀粉变蓝等可准确测定气体的含量,故答案为:bc;
(6)除杂后得到的MnSO4溶液可以通过蒸发浓缩,冷却结晶(过滤)制得硫酸锰晶体;由硫原子守恒,被吸收的SO2的物质的量等于硫酸锰晶体的物质的量,则硫酸锰晶体的质量为
×169g/mol≈20.0kg,
故答案为:蒸发浓缩,冷却结晶(过滤); 20.0.
(1)过滤需要漏斗、烧杯、玻璃棒等,过滤中玻璃棒的作用为引流,防止液体溅出,故答案为:烧杯;漏斗;引流,防止液体溅出;
(2)由于碳酸锰能消耗溶液中的酸,降低溶液的酸性,从而促进Al3+和Fe3+水解生成氢氧化物沉淀,
故答案为:消耗溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀;
(3)当Ni2+恰好完全沉淀 (此时溶液中c(Ni2+)=1.0×10-5mol/L),c(S2-)=
| Ksp(NiS) |
| c(Ni2+) |
| 1.4×10-24 |
| 1×10-5 |
| 8.4×10-45 |
| 1.4×10-19 |
(4)隋性电极作阳极,铁作阴极,则阳极上失去电子发生氧化反应,则阳极反应为MnO42--e-═MnO4-,故答案为:MnO42--e-═MnO4-;
(5)准确测定一定体积燃煤尾气中SO2含量,二氧化硫与氨水、NaOH反应不易控制,且加指示剂现象观察的滴定终点与反应终点误差大,而b、c中利用还原性及高锰酸钾褪色、淀粉变蓝等可准确测定气体的含量,故答案为:bc;
(6)除杂后得到的MnSO4溶液可以通过蒸发浓缩,冷却结晶(过滤)制得硫酸锰晶体;由硫原子守恒,被吸收的SO2的物质的量等于硫酸锰晶体的物质的量,则硫酸锰晶体的质量为
| 1000m3×8.4g/m3×90% |
| 64g/mol |
故答案为:蒸发浓缩,冷却结晶(过滤); 20.0.
点评:本题以物质的制备实验考查混合物分离提纯的综合应用,为高频考点,涉及氧化还原反应、盐类水解、溶度积计算、原子守恒计算等,把握流程分析及混合物分离方法、发生的反应为解答的关键,侧重分析与实验、计算能力的考查,综合性较强,题目难度中等.

练习册系列答案
相关题目
下列离子或分子在溶液中能大量共存,加入足量Na2O2后溶液中仍能大量共存的是( )
| A、K+、Cl-、Na+、SiO32- | ||
B、Ba2+、NO
| ||
| C、K+、Na+、I-、SO42- | ||
D、Na+、Cu2+、NH3.H2O、SO
|
工业上以铬铁矿(主要成分为FeO?Cr2O3)、碳酸钠、氧气、和硫酸为原料生产重铬酸钠(Na2Cr2O7?2H2O),其主要反应为:下列说法正确的是( )
(1)4FeO?Cr2O3+8Na2CO3+7O2
8Na2CrO4+2Fe2O3+8CO2
(2)2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O.
(1)4FeO?Cr2O3+8Na2CO3+7O2
| ||
(2)2Na2CrO4+H2SO4=Na2SO4+Na2Cr2O7+H2O.
| A、反应(1)和(2)均为氧化还原反应 |
| B、反应(1)的氧化剂是O2,还原剂是FeO?Cr2O3 |
| C、高温下,O2的氧化性强于Fe2O3,弱于Na2CrO4 |
| D、反应(1)中每生成1molNa2CrO4时电子转移3mol |
下列解释事实的方程式错误的是( )
| A、测得0.1 mol?L-1氨水的pH为11:NH3?H2O?NH4++OH- | ||||
| B、将Na块投入水中,产生气体:2Na+2H2O═2NaOH+H2↑ | ||||
C、用CuCl2溶液做导电实验,灯泡发光:CuCl2
| ||||
D、将1 mol?L-1FeCl3溶液滴入沸水中,得到透明红褐色液体:FeCl3+3H2O
|






 某温度下,将三种气体充入一密闭容器中,所发生反应的平衡常数可表示为K=
某温度下,将三种气体充入一密闭容器中,所发生反应的平衡常数可表示为K=