题目内容
17.请在横线上填写除杂试剂,并写出相关的离子方程式(1)镁中混有少量铝,试剂:NaOH,离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)铜粉中混有少量铁粉,试剂:HCl,离子方程式:Fe+2H+=Fe2++H2↑;
(3)FeCl2溶液中混有少量的FeCl3,试剂:Fe,离子方程式:2Fe3++Fe=3Fe2+;
(4)氧化铁混有少量氧化铝,试剂:NaOH,离子方程式:2OH-+Al2O3=2AlO2-+H2O;
(5)碳酸氢钠溶液混有少量碳酸钠,试剂:足量CO2,离子方程式:CO32-+CO2+H2O=2HCO3-.
分析 (1)Al与NaOH反应,而Mg不能;
(2)Fe与盐酸反应,而Cu不能;
(3)Fe与氯化铁反应生成氯化亚铁;
(4)氧化铝与NaOH反应,而氧化铁不能;
(5)二氧化碳与碳酸钠、水反应生成碳酸氢钠.
解答 解:(1)Al与NaOH反应,而Mg不能,则选择试剂为NaOH,发生的离子反应为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:NaOH;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)Fe与盐酸反应,而Cu不能,则选择试剂为HCl,发生的离子反应为Fe+2H+=Fe2++H2↑,
故答案为:HCl;Fe+2H+=Fe2++H2↑;
(3)Fe与氯化铁反应生成氯化亚铁,则选择试剂为Fe,发生的离子反应为2Fe3++Fe=3Fe2+
故答案为:Fe;2Fe3++Fe=3Fe2+;
(4)氧化铝与NaOH反应,而氧化铁不能,则选择试剂为NaOH,发生的离子反应为2OH-+Al2O3=2AlO2-+H2O,
故答案为:NaOH;2OH-+Al2O3=2AlO2-+H2O;
(5)二氧化碳与碳酸钠、水反应生成碳酸氢钠,则选择试剂为足量CO2,发生的离子反应为CO32-+CO2+H2O=2HCO3-,
故答案为:足量CO2;CO32-+CO2+H2O=2HCO3-.
点评 本题考查混合物分离提纯及离子反应方程式的书写,为高频考点,把握物质的性质、性质差异及发生的鹅反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案
相关题目
7.关于有机产品 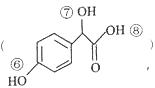 的说法正确的是( )
的说法正确的是( )
 的说法正确的是( )
的说法正确的是( )| A. | Y 既能使溴水褪色又能使酸性高锰酸钾褪色,且原理相同 | |
| B. | Y 的同分异构体中,不存在苯环上的一氯代物只有一种的物质 | |
| C. | 1molY 与氢氧化钠溶液反应时,最多消耗 3mol 氢氧化钠 | |
| D. | Y 中⑥、⑦、⑧三处-OH 的电离程度由大到小的顺序是⑧>⑥>⑦ |
8.A(g)+3B(g)?2C(g)+2D(g),在不同情况下测得反应速率,其中反应最快的是( )
| A. | v(A)=0.3mol/(L•s) | B. | v(B)=0.6 mol/(L•s) | C. | v(C)=0.5 mol/(L•s) | D. | v(D)=0.4mol/(L•s) |
2.下列五种有色溶液与SO2作用均能褪色,其实质相同的是( )
①品红溶液;②酸性KMnO4溶液;③溴水;④滴有酚酞的NaOH溶液.
①品红溶液;②酸性KMnO4溶液;③溴水;④滴有酚酞的NaOH溶液.
| A. | ②③ | B. | ①②③ | C. | ①④ | D. | ②④ |
9.2005年中国防治禽流感药物研究取得重大突破,从中药材提取的金丝桃素对人感染的H5N1亚型禽流感家禽活体具有良好的治愈率.已知金丝桃素的结构简式如下:

下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | 金丝桃素的分子式为C17H22O3N | |
| B. | 金丝桃素能在NaOH溶液中加热反应得到两种芳香族化合物 | |
| C. | 金丝桃素能与浓硫酸和浓硝酸的混合液反应 | |
| D. | 在金属镍催化并加热下,1mol金丝桃素最多能与4molH2发生加成反应 |
6.下列关于酒精的叙述错误的是( )
| A. | 化学名称为乙醇 | B. | 易挥发 | ||
| C. | 常用作有机溶剂 | D. | 不能被酸性高锰酸钾氧化 |
7.化学与生产、生活、社会密切关系,下列说法错误的是( )
| A. | 燃煤发电厂在煤燃烧时加入一些生石灰,能减少废气中的二氧化硫排放 | |
| B. | 洪涝灾害地区的灾民用明矾和漂白粉先后处理浊水后就可直接饮用 | |
| C. | 人们所使用的材料,不一定是纯度越高越好 | |
| D. | 通讯领域中的光导纤维不可长期浸泡在强碱性溶液中 |