题目内容
19.某有机物X的结构简式如图所示,则下列有关说法中不正确的是( )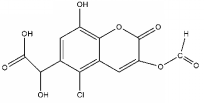
| A. | 能发生加成、取代、氧化反应 | |
| B. | 1 mol该物质最多可与7mol NaOH反应 | |
| C. | 1 mol该物质最多可与6 mol H2反应 | |
| D. | 能与FeCl3溶液发生显色反应 |
分析 有机物含有羧基,具有酸性,可发生中和、酯化反应,含有酚羟基,可发生取代、氧化反应,含有酯基,可发生水解反应,含有氯原子,可发生取代反应,以此解答该题.
解答 解:A.含有苯环,可发生加成反应,含有酚羟基,可发生氧化、取代反应,故A正确;
B.能与氢氧化钠反应的为羧基、酯基、酚羟基和氯原子,且酯基、氯原子可水解生成酚羟基、羧基、HCl,则1 mol该物质最多可与7mol NaOH反应,故B正确;
C.能与氢气发生加成反应的苯环和碳碳双键,则1 mol该物质最多可与4 mol H2反应,故C错误;
D.含有酚羟基,能与FeCl3溶液发生显色反应,故D正确.
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、酯性质的考查,题目难度不大.

练习册系列答案
相关题目
20.用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 等质量的N2和CO所含分子数均为NA | |
| B. | 在标准状况下,22.4L CH4与18g H2O所含的电子数均为10NA | |
| C. | 一定温度下,1L 1mol•L-1的CH3COONa溶液含NA个CH3COO- | |
| D. | 1mol SO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子 |
4.下列是部分短周期中第二、第三周期元素的原子半径及主要化合价.
回答下列问题:
(1)⑧在元素周期表中的位置是第二周期VIA族(周期、族);
(2)8个元素的最高价氧化物的水化物中,酸性最强的是HClO4(填化学式);
(3)元素⑤、⑦、⑧分别形成的简单气态氢化物中,⑦的电子式为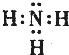 ,稳定性最强的氢化物的结构式为H-O-H;
,稳定性最强的氢化物的结构式为H-O-H;
(4)写出①、④的最高价氧化物对应的水化物之间发生反应的离子方程式Al(OH)3+OH-═AlO2-+2H2O;
(5)用电子式表示元素①与⑥形成化合物的过程 .
.
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +1 | +3 | +5、-3 | +7、-1 | +5、-3 | -2 |
(1)⑧在元素周期表中的位置是第二周期VIA族(周期、族);
(2)8个元素的最高价氧化物的水化物中,酸性最强的是HClO4(填化学式);
(3)元素⑤、⑦、⑧分别形成的简单气态氢化物中,⑦的电子式为
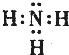 ,稳定性最强的氢化物的结构式为H-O-H;
,稳定性最强的氢化物的结构式为H-O-H;(4)写出①、④的最高价氧化物对应的水化物之间发生反应的离子方程式Al(OH)3+OH-═AlO2-+2H2O;
(5)用电子式表示元素①与⑥形成化合物的过程
 .
.
11.下列化合物中,同分异构体数目超过7个的有( )
| A. | 已烷 | B. | 已烯 | C. | 1,2-二溴丙烷 | D. | 戊醇 |
8.下列说法不正确的是( )
| A. | ${\;}_{6}^{14}$C和${\;}_{6}^{12}$C是同一种核素 | |
| B. | 红磷和白磷互为同素异形体 | |
| C. | CH3COOCH2CH3和CH3CH2COOCH3是不同物质 | |
| D. | CH3CH2OH可看成是由-C2H5和-OH组成 |
9.下列叙述正确的是( )
| A. | 次氯酸的电离方程式为:HClO═H++ClO- | |
| B. | c(H+)等于1×10-7mol•L-1的溶液一定是中性溶液 | |
| C. | 在CH3COONa溶液中,c(CH3COO-)<c(Na+) | |
| D. | 0.2mol•L-1CH3COOH溶液中的c(H+)是0.1mol•L-1 HCl溶液中的c(H+)的2倍 |
 .
. +2H2O.
+2H2O.