题目内容
6.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 4.6g Na与足量氧气反应时转移电子的数目一定为0.2NA | |
| B. | 1mol Cl2参加反应时转移的电子数目为2NA | |
| C. | 1mol KClO3中含有的氯离子数目为NA | |
| D. | 22.4L O2中含有2NA个氧原子 |
分析 A.钠为+1价金属,根据n=$\frac{m}{M}$计算出4.6g钠的物质的量,然后可计算出失去电子的物质的量及数目;
B.氯气与氢氧化钠溶液反应时,1mol氯气完全反应转移了1mol电子;
C.氯酸钾含有钾离子和氯酸根离子,不存在氯离子;
D.没有告诉在标况下,不能使用标况下的气体摩尔体积计算.
解答 解:A.4.6gNa的物质的量为:$\frac{4.6g}{23g/mol}$=0.2mol,0.2mol钠与足量氧气完全反应,无论身处氧化钠还是过氧化钠,失去电子的物质的量一定为0.2mol,转移电子的数目一定为0.2NA,故A正确;
B.1mol Cl2参加反应时,若与氢氧化钠溶液反应,氯气既是氧化剂也是还原剂,转移了1mol电子,转移的电子数目为NA,故B错误;
C.1mol KClO3含有1mol钾离子和1mol氯酸根离子,不存在氯离子,故C错误;
D.不是标准状况下,无法计算22.4L氧气的物质的量,故D错误;
故选A.
点评 本题考查了阿伏伽德罗常数综合应用,题目难度不大,明确标况下气体摩尔体积的使用条件为解答关键,注意掌握物质的量与阿伏伽德罗常数、摩尔质量、气体摩尔体积等物理量之间的关系,试题有利于提高学生的分析能力及化学计算能力.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
16.${\;}_{27}^{60}Co$中60表示( )
| A. | 钴元素的相对原子质量是60 | B. | 钴的一种同位素相对原子质量是60 | ||
| C. | 钴元素的质量为60 | D. | 钴的一种同位素的质量数为60 |
17.在透明水溶液中能大量共存的一组离子是( )
| A. | 酸溶液中Na+、Ba2+、Cl-、NO3-K+ Fe3+ | |
| B. | 使酚酞变红色的溶液:Na+、Cu2+、HCO3-、NO3- | |
| C. | 0.1 mol•L-1AgNO3溶液:H+、K+、SO42-、I- | |
| D. | 0.1 mol•L-1NaAlO2溶液:H+、Na+、Cl-、SO42- |
1.下列反应的离子方程式正确的是( )
| A. | 氢氧化钡溶液中滴加稀硫酸:Ba2++SO42-═BaSO4↓ | |
| B. | 碳酸钙与稀硝酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | 向较浓的Na2SiO3溶液中滴加适量盐酸制得硅酸胶体:SiO32-+2H+=H2SiO3(胶体) | |
| D. | 向氯化铝溶液中加过量氨水:A13++4NH3•H2O=AlO2-+2H2O+4NH4+ |
11.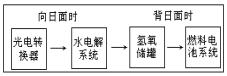 如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH溶液为电解液,下列有关说法中不正确的是( )
如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH溶液为电解液,下列有关说法中不正确的是( )
 如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH溶液为电解液,下列有关说法中不正确的是( )
如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH溶液为电解液,下列有关说法中不正确的是( )| A. | 该能量转化系统中的水也是可能循环的 | |
| B. | 燃料电池系统产生的能量实际上来自于水 | |
| C. | 水电解系统中的阳极有O2放出 | |
| D. | 燃料电池放电时的负极反应:H2+2OH--2e-=2H2O |
18.下列物质的水解产物都是葡萄糖的是( )
①蔗糖②果糖③淀粉④纤维素⑤油脂.
①蔗糖②果糖③淀粉④纤维素⑤油脂.
| A. | ①②③④ | B. | ①③④ | C. | ③④ | D. | ③④⑤ |
15.下列物质长期置于空气中质量不会增加的是( )
| A. | NaOH固体 | B. | 浓H2SO4 | C. | 碳酸钠晶体 | D. | Na2SO3溶液 |
19.下列物质中能导电,但又不是电解质和非电解质的纯净物是( )
| A. | 熔融的NaCl | B. | 石墨晶体 | C. | 液氯 | D. | 盐酸 |
 A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).