题目内容
配平离子方程式:
KMnO4-+ H2O2+ ═ Mn2++ O2↑+ H2O.
考点:氧化还原反应方程式的配平
专题:氧化还原反应专题
分析:根据氧化还原反应中得失电子数相等配平方程式.
解答:
解:反应中物质的化合价变化:MnO4-→Mn2+,Mn元素化合价由+7价→+2价,一个MnO4-得5个电子;H2O2→O2,
O由-1价变成0价,一个H2O2分子失去2个电子,所以其最小公倍数为10,故MnO4-的计量数为2,双氧水的计量数为5,然后根据原子守恒配平其它元素.
所以其方程式为:2KMnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O
故答案为:2;5;6H+;2;5;8.
O由-1价变成0价,一个H2O2分子失去2个电子,所以其最小公倍数为10,故MnO4-的计量数为2,双氧水的计量数为5,然后根据原子守恒配平其它元素.
所以其方程式为:2KMnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O
故答案为:2;5;6H+;2;5;8.
点评:本题考查了离子方程式的配平,要掌握用得失电子数相等来配平的方法.

练习册系列答案
相关题目
下列有关离子方程式书写正确的( )
| A、在强碱溶液中次氯酸钠与Fe(0H)3反应生成Na2FeO4:3ClO-+2Fe(0H)3=2FeO42-+3Cl-+H2O+4H+ |
| B、从酸化的海带灰浸出液中提取碘:2I-+H2O2=I2+2OH- |
| C、以金属银为阳极电解饱和硫酸铜溶液:Cu2++2 H2O=2Cu+O2 ↑+4H+ |
| D、过氧化氢能使酸性KMnO4溶液褪色:5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O |
下列有关化学用语表示正确的是( )
A、对硝基甲苯的结构简式: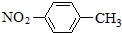 | ||
B、氯化铵的电子式: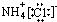 | ||
C、中子数为16的硫原子:
| ||
| D、乙炔的最简式:CH |
下列物质按照纯净物、混合物、电解质和非电解质顺序排列的是( )
| A、盐酸、天然气、醋酸、干冰 |
| B、胆矾、漂白粉、氯化钾、氯气 |
| C、氯化钠、福尔马林、硫酸钠、乙醇 |
| D、单甘油酯、混甘油酯、苛性钾、石灰 |
 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.如图为RFC工作原理示意图,有关说法正确的是( )
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.如图为RFC工作原理示意图,有关说法正确的是( )| A、转移0.1mol电子时,a电极产生1.12LH2(标准状况) |
| B、b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH- |
| C、c电极上进行还原反应,B电池中的H+可以通过隔膜进入A池 |
| D、d电极上发生的电极反应是:O2+4H++4e-=2H2O |
在给定条件下,下列划横线的物质在化学反应中能被完全消耗的是( )
| A、标准状况下,将1g铝片投入20mL 18.4mol?L-1的硫酸中 |
| B、向100mL3moI?L-1的硝酸中加入5.6g铁 |
| C、用50mL18mol?L-1浓硫酸与足量Cu共热(指其中的硫酸被完全消耗) |
| D、在5×107 Pa、500℃和铁触媒催化的条件下,用3mol氢气和2mol氮气合成氨 |
在标准状况下,与12g H2体积相同的氮气的( )
| A、质量是168 g |
| B、物质的量是6 mol |
| C、体积约为134.4 L |
| D、物质的量为12 mol |