题目内容
6.除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 乙烷(乙烯) | 氢气 | 加热 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| D | 淀粉(氯化钠) | 蒸馏水 | 渗析 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.苯与三溴苯酚、溴不分层,无法通过过滤分离;
B.无法可知氢气的量,易导致引进杂质氢气;
C.乙酸乙酯和乙酸都与氢氧化钠溶液反应;
D.淀粉和氯化钠分别溶于水形成胶体、溶液,结合胶体和溶液的分散质粒子大小分析.
解答 解:A.苯是有机溶剂,生成的三溴苯酚能够溶于苯,不会生成沉淀,则无法用过滤操作分离,可用氢氧化钠溶液通过分液操作分离,故A错误;
B.乙烯与氢气反应生成乙烷,但是不易可知氢气的量,应该用溴水除去乙烷中的乙烯,故B错误;
C.二者都与NaOH溶液反应,违反了除杂原则,可用饱和碳酸氢钠溶液除去乙酸乙酯中的乙酸,故C错误;
D.淀粉和氯化钠分别溶于水形成胶体、溶液,胶体粒子不会透过半透膜,可通过渗析操作分离,故D正确;
故选D.
点评 本题考查物质分离与提纯、化学实验方案的评价,题目难度中等,明确常见化学实验基本操作方法即可解答,注意掌握物质分离与提纯方法,试题培养了学生的化学实验能力.

练习册系列答案
相关题目
1.设NA表示阿伏伽德罗常数,正确的是( )
| A. | 20°C时,28g N2所含的原子数为2NA个 | |
| B. | 标况下,0.5NA个水分子所占体积约为11.2L | |
| C. | CH4的摩尔质量在数值上等于NA个甲烷分子的质量之和 | |
| D. | 1gCO与1gCO2所含碳原子数之比是1:1 |
2.下列离子方程式与所述事实相符的是( )
| A. | Na2S2O3溶液中加入稀盐酸:2S2O32-+2H+=SO42-+3S+H2O | |
| B. | 将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-=SO32-+2HClO | |
| C. | 向含有0.4molFeBr2的溶液中通入0.3molCl2充分反应4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 | |
| D. | 向Al2(SO4)3溶液中加入过量氨水:Al3++4NH3•H2O=AlO2-+4NH4+ |
19.下列说法正确的是( )
| A. | 由原子构成的晶体不一定是原子晶体 | |
| B. | 分子晶体中的分子间可能含有共价键 | |
| C. | 分子晶体中一定有共价键 | |
| D. | 分子晶体中分子一定紧密堆积 |
1.无机化合物可根据其组成和性质进行分类:
(1)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在表②③⑥的后面.
(2)写出⑦转化为⑤的化学方程式2NaOH+CO2═Na2CO3+H2O.
(3)实验室制备⑦常用石灰石和盐酸反应,检验该气体的方法是Ca(OH)2+CO2═CaCO3+H2O.(化学方程式)
(1)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在表②③⑥的后面.
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 | ①HCl ②H2SO4 | ③NaOH ④Ba(OH)2 | ⑤Na2CO3 ⑥K2CO3 | ⑦CO2 ⑧Na2O2 |
(3)实验室制备⑦常用石灰石和盐酸反应,检验该气体的方法是Ca(OH)2+CO2═CaCO3+H2O.(化学方程式)
11.由于少数不法商贩惟利是图,假酒、假盐、假药等引起的中毒事件屡有发生.下列物质被误食后,不会引起中毒的是( )
| A. | NaNO2 | B. | AgNO3 | C. | BaCO3 | D. | BaSO4 |
18.在盛有稀碳酸钠溶液的烧杯中插入惰性电极,电解一时间后,溶液中无晶体析出,则下列说法错误的是( )
| A. | 溶液的浓度增大 | |
| B. | 溶液的pH增大 | |
| C. | 溶液中钠离子与碳酸根离子的物质的量之比变小 | |
| D. | 溶液的质量分数不变 |
16.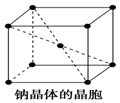 金属钠晶体为体心立方晶格(如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(molC-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
金属钠晶体为体心立方晶格(如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(molC-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
 金属钠晶体为体心立方晶格(如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(molC-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
金属钠晶体为体心立方晶格(如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(molC-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )| A. | $\root{3}{\frac{2a}{{N}_{A}ρ}}$ | B. | $\sqrt{2}$$\root{3}{\frac{2a}{{N}_{A}ρ}}$ | C. | $\frac{\sqrt{3}}{4}$$\root{3}{\frac{2a}{{N}_{A}ρ}}$ | D. | $\frac{1}{2}$$\root{3}{\frac{2a}{{N}_{A}ρ}}$ |
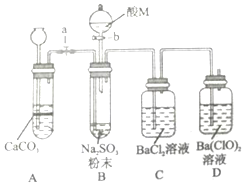 SO2是一种有毒气体,但可用于酒精的防腐剂,可以抵抗微生物的侵袭.甲同学用Na2SO4制备SO2,并验证SO2的部分性质.设计了如下实验步骤及装置:
SO2是一种有毒气体,但可用于酒精的防腐剂,可以抵抗微生物的侵袭.甲同学用Na2SO4制备SO2,并验证SO2的部分性质.设计了如下实验步骤及装置: