题目内容
某温度下,密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如下表 ,下列说法错误的是( )
,下列说法错误的是( )
A.反应达到平衡时,X的转化率为80%
 B.该反应的平衡常数表达式为K=
B.该反应的平衡常数表达式为K=
C.增大压强其平衡常数不变,但使平衡向生成Z的方向移动
 D.改变温度可以改变此反应的平衡常数
D.改变温度可以改变此反应的平衡常数
 ,下列说法错误的是( )
,下列说法错误的是( )| 物质 | X | Y | Z | W |
| 初始浓度/mol·L-1 | 0.5 | 0.6 | 0 | 0 |
| 平衡浓度/mol·L-1 | 0.1 | 0.1 | 0.4 | 0.6 |
 B.该反应的平衡常数表达式为K=
B.该反应的平衡常数表达式为K=
C.增大压强其平衡常数不变,但使平衡向生成Z的方向移动
 D.改变温度可以改变此反应的平衡常数
D.改变温度可以改变此反应的平衡常数C
根据表中数据可知,平衡时消耗X的物质的量浓度是(0.5-0.1)mol/L=0.4mol/L,所以X的转化率是 ,A正确。X、Y、Z、W变化量之比是0.4︰0.5︰0.4︰0.6=4︰5︰4︰6,即反应的方程式为4X+5Y
,A正确。X、Y、Z、W变化量之比是0.4︰0.5︰0.4︰0.6=4︰5︰4︰6,即反应的方程式为4X+5Y 4Z+6W,所以选项B正确。正反应是体积增大的可逆反应,所以增大压强平衡向逆反应方向移动,C不正确。平衡常数和温度有关,D正确。所以答案选C。
4Z+6W,所以选项B正确。正反应是体积增大的可逆反应,所以增大压强平衡向逆反应方向移动,C不正确。平衡常数和温度有关,D正确。所以答案选C。
 ,A正确。X、Y、Z、W变化量之比是0.4︰0.5︰0.4︰0.6=4︰5︰4︰6,即反应的方程式为4X+5Y
,A正确。X、Y、Z、W变化量之比是0.4︰0.5︰0.4︰0.6=4︰5︰4︰6,即反应的方程式为4X+5Y 4Z+6W,所以选项B正确。正反应是体积增大的可逆反应,所以增大压强平衡向逆反应方向移动,C不正确。平衡常数和温度有关,D正确。所以答案选C。
4Z+6W,所以选项B正确。正反应是体积增大的可逆反应,所以增大压强平衡向逆反应方向移动,C不正确。平衡常数和温度有关,D正确。所以答案选C。
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
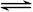 3C(g)+D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。
3C(g)+D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。 HSO3-+OH-水解平衡的事实是 _(填序号)。
HSO3-+OH-水解平衡的事实是 _(填序号)。
 2SO3(g),
2SO3(g), 下列叙述能够说明反应已经达到平衡状态的是( )
下列叙述能够说明反应已经达到平衡状态的是( )
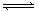 pC(g)+qD(g),根据图回答:
pC(g)+qD(g),根据图回答:
 R(g)+2L,此反应符合下图关系,该反应是下列哪种情况
R(g)+2L,此反应符合下图关系,该反应是下列哪种情况
 xC(g)+ 2D(g)。2min末该反应达到平衡,生成0.8mol D ,并测得C的浓度为0.2mol·L-1。请填空:
xC(g)+ 2D(g)。2min末该反应达到平衡,生成0.8mol D ,并测得C的浓度为0.2mol·L-1。请填空:
 (1)2 min时,容器内n(N2)== ,c(H2)== 。
(1)2 min时,容器内n(N2)== ,c(H2)== 。
 (3)2 min时,容器内气体的总物质的量与反应前容器内气体的总物质的量之比为:
(3)2 min时,容器内气体的总物质的量与反应前容器内气体的总物质的量之比为: