题目内容
7.NA为阿伏伽德罗常数的值,下列说法正确的是( )| A. | 16g由O2和O3的混合气体中含有的分子数为0.5NA | |
| B. | 2.3g金属钠在装有氧气的集气瓶中完全燃烧,转移的电子数为0.1NA | |
| C. | 100mL 12mol/L浓盐酸与足量MnO2共热,生成的Cl2分子数为0.3NA | |
| D. | 标准状况下,22.4LSO3含有的分子数为NA个 |
分析 A.氧气与臭氧摩尔质量不同;
B.钠与氧气反应无论生成氧化钠还是过氧化钠,钠都变为+1价离子;
C.二氧化锰与浓盐酸反应,与稀盐酸不反应;
D.气体摩尔体积使用对象为气体.
解答 解:A.氧气与臭氧摩尔质量不同,只知道混合物质量,无法计算混合物物质的量,含有分子的数,故A错误;
B.2.3g金属钠物质的量为$\frac{2.3g}{23g/mol}$=0.1mol,在装有氧气的集气瓶中完全燃烧,生成0.1mol钠离子,转移的电子数为0.1NA,故B正确;
C.100mL 12mol/L浓盐酸与足量MnO2共热,随着反应进行,盐酸浓度降低变为稀盐酸,不与二氧化锰反应,所以生成的Cl2分子数小于0.3NA,故C错误;
D.标况下三氧化硫不是气体,不能用气体摩尔体积,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的有关计算及应用判断,掌握以物质的量为核心的计算公式,熟悉物质的结构组成是解题关键,难度不大,注意气体摩尔体积使用条件和对象.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.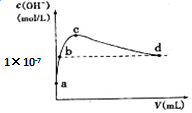 常温下,向1 L pH=10的NaOH溶液中持续通入CO2.通入CO2的体积(V)与溶液中水电离出的c(OH-)的关系如图所示.下列叙述不正确的是( )
常温下,向1 L pH=10的NaOH溶液中持续通入CO2.通入CO2的体积(V)与溶液中水电离出的c(OH-)的关系如图所示.下列叙述不正确的是( )
 常温下,向1 L pH=10的NaOH溶液中持续通入CO2.通入CO2的体积(V)与溶液中水电离出的c(OH-)的关系如图所示.下列叙述不正确的是( )
常温下,向1 L pH=10的NaOH溶液中持续通入CO2.通入CO2的体积(V)与溶液中水电离出的c(OH-)的关系如图所示.下列叙述不正确的是( )| A. | d点溶液中:c(Na+)═2c(CO32-)+c(HCO3-) | |
| B. | c点溶液中:c(Na+)>c(HCO3-)>c(CO32-) | |
| C. | b点溶液中:c(H+)=1×10-7mol•L-1 | |
| D. | a点溶液中:水电离出的c(H+)=1×10-10mol•L-1 |
18.下列关于元素金属性与非金属性的说法正确的是( )
| A. | 元素X位于元素Y的上一个周期,则元素X的非金属性元素比元素Y强 | |
| B. | 测定相同条件下的Na2CO3和Na2SO4的pH,可以比较碳与硫的非金属性强弱 | |
| C. | 非金属性元素的最高价氧化物对应的水化物稳定性越强,则非金属性越强 | |
| D. | 发生氧化还原反应时,X原子失去的电子比Y原子多,证明X的金属性一定比Y强 |
15.下列有关元素及其化合物的叙述正确的是( )
| A. | Fe( OH)3胶体无色、透明,能发生丁达尔现象 | |
| B. | CO2通入CaCl2溶液中生成CaCO3沉淀 | |
| C. | 将稀硫酸滴加到Fe( NO3)2溶液中无明显现象 | |
| D. | H2、SO2、CO2三种气体都可以用浓硫酸干燥 |
2.在给定条件下,下列选项所示的物质间转化均能一步实现的是(
| A. | S$→_{点燃}^{足量O_{2}}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| B. | SiO2$\stackrel{盐酸}{→}$SiCl4$→_{高温}^{H_{2}}$Si | |
| C. | NH3$→_{催化剂、△}^{O_{2}}$NO$\stackrel{O_{2}}{→}$NO2 | |
| D. | Fe$→_{点燃}^{少量Cl_{2}}$FeCl2$\stackrel{NaOH溶液}{→}$Fe(OH)2 |
12.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液中:Fe2+、NO3-、Na+、SO42- | |
| B. | c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、Cl-、NO3- | |
| C. | 水电离出的c(H+)=10-12mol/L的溶液中:Ca2+、K+、Cl-、HCO3- | |
| D. | c(Fe3+)=0.1 mol/L的溶液中:K+、ClO-、SO42-、SCN- |
19.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 摩尔是国际单位制七个基本物理量之一 | |
| B. | 1 L 0.1 mol/L BaCl2溶液中所含的Cl-为0.1 NA | |
| C. | 常温常压下,11.2 L Cl2所含的分子数为0.5 NA | |
| D. | 常温常压下,32 g O2含有的氧原子数为2 NA |
16.下列实验现象与氧化还原反应有关的是( )
| A. | 向碳酸钠溶液中滴加氯化钙溶液,产生白色沉淀 | |
| B. | 向含有酚酞的氢氧化钠溶液中滴加盐酸,红色褪去 | |
| C. | 向硅酸钠溶液中通入二氧化碳,产生白色胶状沉淀 | |
| D. | 硫酸铜溶液中插入铁片,铁片上出现红色物质 |