题目内容
4.用惰性电极进行电解,下列说法正确的是( )| A. | 电解稀硫酸溶液,实质上是电解水,故溶液pH不变 | |
| B. | 电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小 | |
| C. | 电解硫酸铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:2 | |
| D. | 电解氯化铜溶液,消耗完氯化铜后电解就会停止 |
分析 A、电解硫酸溶液,在阴极上和阳极上析出产物分别是氢气和氧气;
B、电解稀氢氧化钠溶液,实质上是电解水,氢氧化钠溶液的浓度变大;
C、电解硫酸钠溶液,实质电解水,阳极生成氧气,阴极生成Cu;
D、电解氯化铜溶液,生成铜和氯气.
解答 解:A、电解硫酸溶液,在阴极上和阳极上析出产物分别是氢气和氧气,实质上是电解水,溶液pH减小,故A错误;
B、电解稀氢氧化钠溶液,实质是电解水,氢氧化钠溶液的浓度变大,溶液pH增大,故B错误;
C、电解硫酸铜溶液,阳极生成氧气,阴极生成铜,阴极上和阳极上析出产物的物质的量之比为2:1,故C错误;
D、电解氯化铜溶液,生成铜和氯气,在阴极上和阳极上析出产物分别是铜和氯气,消耗完氯化铜后剩余的是水,电解就会停止,故D正确;
故选D.
点评 本题考查学生电解池的工作原理知识,注意离子的放电顺序是关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列属于氧化物的是( )
| A. | H2SO4 | B. | Ca(OH)2 | C. | KClO3 | D. | CO 2 |
19.固体X中可能含有MgCl2、Na2CO3、K2SO3、KAlO2中的一种或几种.为确定该固体粉末的成分,现取X进行下列实验,实验过程及现象如下:

根据上述实验,下列说法正确的是( )

根据上述实验,下列说法正确的是( )
| A. | 气体1可能为SO2和CO2的混合物 | |
| B. | 沉淀3可能为Al(OH)3 | |
| C. | 沉淀4可能为BaCO3、BaSO3或二者混合物 | |
| D. | 固体粉末X中一定有Na2CO3,可能有KAlO2 |
9.已知15g A物质和10.5g B物质恰好完全反应生成7.2g C、1.8g D和0.3mol E,则物质E的摩尔质量是( )
| A. | 55 mol•g-1 | B. | 55 mol | C. | 55 g•mol-1 | D. | 55g |
16.下列有关化学用语表示正确的是( )
| A. | 乙炔的电子式: | B. |  和 和 是同一物质 是同一物质 | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 乙烯的球棍模型: |
13.前不久,我国科学家合成了三种新核素,其中一种是${\;}_{72}^{185}$Hf.下列关于${\;}_{72}^{185}$Hf的叙述中,正确的是( )
| A. | 该元素的原子序数是72 | B. | 该元素的原子序数是113 | ||
| C. | 该核素的中子数为72 | D. | 该元素的相对原子质量为了185 |
14.能正确表示下列反应的离子方程式为( )
| A. | 向FeI2溶液中滴入过量溴水:2Fe2++2I-+2Br2=2Fe3++I2+4Br- | |
| B. | NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | |
| C. | 用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| D. | 向FeCl3溶液中加入少量KSCN溶液:Fe3++3SCN-=Fe(SCN)3↓ |
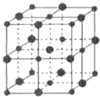 已知X、Y、Z、M、Q五种元素的原子序数依次递增;X、Y、M三种元素组成的一种化合物A是新装修居室中常含有的一种有害气体.Q4+离子和氩原子的核外电子排布相同.
已知X、Y、Z、M、Q五种元素的原子序数依次递增;X、Y、M三种元素组成的一种化合物A是新装修居室中常含有的一种有害气体.Q4+离子和氩原子的核外电子排布相同.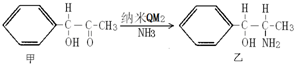
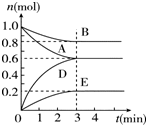 T℃、2L密闭容器中某一反应在不同时刻的各物质的量如图所示(E为固体,其余为气体).回答下列问题.
T℃、2L密闭容器中某一反应在不同时刻的各物质的量如图所示(E为固体,其余为气体).回答下列问题.