题目内容
5.如图是元素周期表中短周期的一部分,若A原子最外层的电子数比次外层少3,则下列说法正确的是( )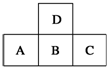
| A. | 原子半径的大小顺序是C>B>A>D | |
| B. | B、D之间只能形成一种化合物 | |
| C. | 只有A的单质存在同素异形体 | |
| D. | A、B、C的最高价氧化物对应水化物的酸性强弱的关系是C>B>A |
分析 由短周期元素A、B、C、D相对位置,可知D处于第二周期,A、B、C处于第三周期,A原子最外层的电子数比次外层少3,最外层电子数为5,故A为P元素,B为S元素,C为Cl,D为O元素,结合元素周期律与元素化合物知识解答.
解答 解:由短周期元素A、B、C、D相对位置,可知D处于第二周期,A、B、C处于第三周期,A原子最外层的电子数比次外层少3,最外层电子数为5,故A为P元素,B为S元素,C为Cl,D为O元素.
A.同周期自左而右原子半径减小,一般电子层越多原子半径越大,故原子半径的大小顺序是A>B>C>D,故A错误;
B.氧、硫之间可以形成二氧化硫、三氧化硫,故B错误;
C.氧元素存在同素异形体氧气、臭氧,故C错误;
D.同周期自左而右非金属性增强,最高价氧化物对应水化物的酸性增强,故D正确.
故选:D.
点评 本题考查结构性质位置关系应用,熟练掌握元素周期表的结构与核外电子排布规律,理解元素周期律.

练习册系列答案
相关题目
15.下列说法中错误的是( )
| A. | 需要加热才能发生的反应不一定是吸收热量的反应 | |
| B. | 科学家经常在金属与非金属的交界线处寻找良好的半导体材料 | |
| C. | 催化剂是影响化学反应速率和化学平衡的一个重要因素 | |
| D. | 物质燃烧可看做“储存”在物质内部的能量(化学能)转化为热能释放出来 |
16.法国里昂的科学家最近发现一种只由四个中子组成的微粒,这种微粒称为“四中子”,也有人称之为“零号元素”.它与天体中的中子星构成类似.有关:“四中子”微粒的说法正确的( )
| A. | 该微粒的质量数为2 | |
| B. | 该微粒不显电性 | |
| C. | 它与普通中子互称为同位素 | |
| D. | 在元素周期表中与氢元素占同一位置 |
13.与 3-甲基-1-戊烯同属烯烃且主链为4个碳的同分异构体共有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
20.甲烷与氯气发生取代反应,生成的四种不同的氯代物中,分子结构为正四面体型的是( )
| A. | CH3Cl | B. | CH2Cl2 | C. | CHCl3 | D. | CCl4 |
10.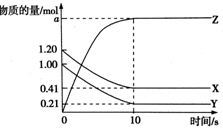 已知可逆反应X(g)+Y(g)?2Z(g),在容积为2L 的密闭容器中反应,有关物质的物质的量的变化如图所示.下列叙述正确的是( )
已知可逆反应X(g)+Y(g)?2Z(g),在容积为2L 的密闭容器中反应,有关物质的物质的量的变化如图所示.下列叙述正确的是( )
 已知可逆反应X(g)+Y(g)?2Z(g),在容积为2L 的密闭容器中反应,有关物质的物质的量的变化如图所示.下列叙述正确的是( )
已知可逆反应X(g)+Y(g)?2Z(g),在容积为2L 的密闭容器中反应,有关物质的物质的量的变化如图所示.下列叙述正确的是( )| A. | a为1.60 | |
| B. | X和Y的转化率相等 | |
| C. | 0~10min的平均速率V(Z)=0.079mol•L-1•min-1 | |
| D. | 容器内Z的浓度最大可以达到1.00 mol/L |
17.历史最久的海水淡化方法是( )
| A. | 蒸馏法 | B. | 电渗析法 | C. | 离子交换法 | D. | 过滤法 |
14.含有共价键的分子晶体是( )
| A. | NaOH | B. | SiO2 | C. | Cl2 | D. | NH4Cl |
 ;若XY2为共价化合物时,其结构式为:S=C=S.
;若XY2为共价化合物时,其结构式为:S=C=S.