题目内容
下列各组物质中所含分子数一定相同的是( )
| A、标准状况下1mol 水和22.4L CO2 |
| B、标准状况下2gH2和22.4L溴 |
| C、0.1mol HCl和2.24L He |
| D、28g CO和6.02×1023个CO分子 |
考点:物质的量的相关计算
专题:计算题
分析:所含分子数一定相同,说明二者的物质的量相等,根据n=
=
=
计算其物质的量.
| V |
| Vm |
| m |
| M |
| N |
| NA |
解答:
解:所含分子数一定相同,说明二者的物质的量相等,
A.标况下,22.4L二氧化碳的物质的量是1mol,水和二氧化碳的物质的量相等,所以其分子数一定相等,故A正确;
B.标况下,溴是液体,气体摩尔体积对其不适用,所以无法计算溴的物质的量,导致无法判断二者物质的量是否相等,无法确定其分子个数是否相等,故B错误;
C.温度、压强未知,导致无法计算He的物质的量,则无法判断二者分子数是否相等,故C错误;
D.28gCO的物质的量=
=1mol,6.02×1023个CO分子的物质的量=
=1mol,二者的物质的量相等,则其分子个数一定相等,故D正确;
故选AD.
A.标况下,22.4L二氧化碳的物质的量是1mol,水和二氧化碳的物质的量相等,所以其分子数一定相等,故A正确;
B.标况下,溴是液体,气体摩尔体积对其不适用,所以无法计算溴的物质的量,导致无法判断二者物质的量是否相等,无法确定其分子个数是否相等,故B错误;
C.温度、压强未知,导致无法计算He的物质的量,则无法判断二者分子数是否相等,故C错误;
D.28gCO的物质的量=
| 28g |
| 28g/mol |
| 6.02×1023 |
| 6.02×1023/mol |
故选AD.
点评:本题考查了物质的量的有关计算,明确气体摩尔体积的适用范围及适用条件是解本题关键,熟练掌握基本公式即可解答,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
1mol?L-1硫酸溶液的含义是( )
| A、1 L水中含有1 mol硫酸 |
| B、1 L溶液中含1 mol H+ |
| C、将98 g硫酸溶于1 L水所配成的溶液 |
| D、指1 L硫酸溶液中含有98 g H2SO4 |
 X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是( )| A、原子半径:W>Z>Y>X |
| B、相等物质的量浓度的气态氢化物溶液的pH:X>Z>W |
| C、最高价氧化物对应水化物的酸性:Z>W>X |
| D、四种元素的单质中,Z单质的熔沸点最低 |
下列关于电解池的叙述中不正确的是( )
| A、与电源正极相连的是电解池的阴极 |
| B、与电源负极相连的是电解池的阴极 |
| C、在电解池的阳极发生氧化反应 |
| D、电子从电源的负极沿导线流入电解池的阴极 |
标准状况下,相同物质的量的CO和CO2,下列有关说法正确的是( )
| A、具有相同数目的原子数 |
| B、具有相同的氧原子数 |
| C、具有相同的质量 |
| D、质量比为7:11 |
将等体积的0.1mol?L-1 KHSO4溶液逐滴加入0.1mol?L-1的Na2SO3溶液中,所得溶液能使紫色石蕊试液变红,则下列各离子浓度关系中不正确的是( )
A、c(SO
| ||||||
| B、c(Na+)>c(K+)>c(H+)>c(OH-) | ||||||
C、c(Na+)=c(SO
| ||||||
D、c(Na+)+c(K+)+c(H+)=2c(SO
|
下列各组反应中,前者属于取代反应,后者则属于加成反应的是( )
| A、乙酸、乙醇和浓H2SO4混合共热;乙醛和Cu(OH)2悬浊液共热 |
| B、乙醇和浓H2SO4加热到170℃;乙醇与灼热的铜反应 |
| C、苯酚溶液中滴加溴水;乙烯通入溴水 |
| D、苯和氢气在镍催化下加热反应;苯和液溴、铁粉混合 |
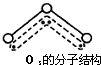 ,呈V型,键角116.5℃.三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键--三个O原子均等地享有这4个电子.请回答:
,呈V型,键角116.5℃.三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键--三个O原子均等地享有这4个电子.请回答: