题目内容
1994年度诺贝尔化学奖授予为研究臭氧作出特殊贡献的化学家.O3能吸收有害紫外线,保护人类赖以生存的空间.O3分子的结构如图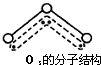 ,呈V型,键角116.5℃.三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键--三个O原子均等地享有这4个电子.请回答:
,呈V型,键角116.5℃.三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键--三个O原子均等地享有这4个电子.请回答:
(1)臭氧与氧气的关系是 .
(2)下列与O3分子的结构相似的是 .
A.H3O+ B.CO2 C.SO2D.BeCl2E.NO2-
(3)分子中某原子有1对没有跟其他原子共用的价电子叫孤对电子,那么O3分子有 对孤对电子.
(4)O3分子是否为极性分子 (是或否).
 ,呈V型,键角116.5℃.三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键--三个O原子均等地享有这4个电子.请回答:
,呈V型,键角116.5℃.三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键--三个O原子均等地享有这4个电子.请回答:(1)臭氧与氧气的关系是
(2)下列与O3分子的结构相似的是
A.H3O+ B.CO2 C.SO2D.BeCl2E.NO2-
(3)分子中某原子有1对没有跟其他原子共用的价电子叫孤对电子,那么O3分子有
(4)O3分子是否为极性分子
考点:判断简单分子或离子的构型,极性分子和非极性分子
专题:化学键与晶体结构
分析:(1)臭氧是由3个氧原子构成的分子;O2和O3都是由氧元素形成的不同单质,互为同素异形体;
(2)根据分子中中心原子的价层电子对数判断分子的空间构型;
(3)根据孤对电子的概念及臭氧分子结构分析;
(4)分子中正负电荷中心不重合,这样的分子为极性分子;分子中正负电荷的重心重合,则为非极性分子.
(2)根据分子中中心原子的价层电子对数判断分子的空间构型;
(3)根据孤对电子的概念及臭氧分子结构分析;
(4)分子中正负电荷中心不重合,这样的分子为极性分子;分子中正负电荷的重心重合,则为非极性分子.
解答:
解:(1)由同种元素形成的不同种单质互为同素异形体,1个臭氧分子是由3个氧原子构成,化学式为:O3;O2和O3都是由氧元素形成的不同单质,互为同素异形体,
故答案为:同素异形体;
(2)O3分子的结构如图 ,在臭氧O3中,中心的氧原子以sp2杂化,与两旁的配位氧原子键合生成两个σ键,使O3分子呈V形;
,在臭氧O3中,中心的氧原子以sp2杂化,与两旁的配位氧原子键合生成两个σ键,使O3分子呈V形;
A.H3O+中含有3对σ键,1对孤电子对,O原子sp3杂化,空间结构为三角锥形,故A错误;
B.CO2为含有4个σ键,没有孤电子对,为sp杂化,空间结构为直线形,故B错误;
C.SO2分子呈“V”字形结构,其成键方式与O3类似,S原子sp2杂化,S原子和两侧的氧原子除以σ键结合以外,还形成一个三中心四电子的大π键,故C正确;
D.BeCl2含有2个σ键,没有孤电子对,为sp杂化,空间结构为直线形,故D错误;
E.NO2-中O含有2个σ键,1对孤电子对,为sp2杂化,空间结构为V形,故E正确;
故答案为:CE;
(3)臭氧分子中,中间的氧原子含有1对孤电子对,两边的各含有2对孤电子对,所以总共5对孤电子对,
故答案为:5;
(4)O3中的中心O原子为sp2杂化,理想模型为平面三角形,分子构型为V型,而且O3形成的是三中心四电子大π键,空间构型不对称.正负电荷重心不重合,所以是极性分子;
故答案为:是.
故答案为:同素异形体;
(2)O3分子的结构如图
 ,在臭氧O3中,中心的氧原子以sp2杂化,与两旁的配位氧原子键合生成两个σ键,使O3分子呈V形;
,在臭氧O3中,中心的氧原子以sp2杂化,与两旁的配位氧原子键合生成两个σ键,使O3分子呈V形;A.H3O+中含有3对σ键,1对孤电子对,O原子sp3杂化,空间结构为三角锥形,故A错误;
B.CO2为含有4个σ键,没有孤电子对,为sp杂化,空间结构为直线形,故B错误;
C.SO2分子呈“V”字形结构,其成键方式与O3类似,S原子sp2杂化,S原子和两侧的氧原子除以σ键结合以外,还形成一个三中心四电子的大π键,故C正确;
D.BeCl2含有2个σ键,没有孤电子对,为sp杂化,空间结构为直线形,故D错误;
E.NO2-中O含有2个σ键,1对孤电子对,为sp2杂化,空间结构为V形,故E正确;
故答案为:CE;
(3)臭氧分子中,中间的氧原子含有1对孤电子对,两边的各含有2对孤电子对,所以总共5对孤电子对,
故答案为:5;
(4)O3中的中心O原子为sp2杂化,理想模型为平面三角形,分子构型为V型,而且O3形成的是三中心四电子大π键,空间构型不对称.正负电荷重心不重合,所以是极性分子;
故答案为:是.
点评:本题考查了臭氧分子的空间构型的判断,注意根据分子的中心原子的价层电子对数判断,题目难度中等.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下列各组物质中所含分子数一定相同的是( )
| A、标准状况下1mol 水和22.4L CO2 |
| B、标准状况下2gH2和22.4L溴 |
| C、0.1mol HCl和2.24L He |
| D、28g CO和6.02×1023个CO分子 |


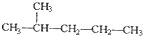 和
和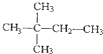 ②
② 和
和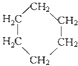
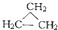 ④C2H6和
④C2H6和 ⑤
⑤ 和
和