��Ŀ����
18�����й��ڷ�Ӧ�ȵ�˵����ȷ���ǣ�������| A�� | ����HΪ��-��ʱ����ʾ�÷�ӦΪ���ȷ�Ӧ | |
| B�� | ��ѧ��Ӧ�ķ�Ӧ��ֻ�뷴Ӧ��ϵ��ʼ̬����̬�йأ����뷴Ӧ��;���� | |
| C�� | H2S��ȼ���ȡ�H=-a kJ•mol-1�����ʾH2Sȼ���ȵ��Ȼ�ѧ����ʽΪ2H2S��g��+3O2��g���T2SO2��g��+2H2O��l����H=-2a kJ•mol-1 | |
| D�� | ��Ӧ�ȵĴ�С�뷴Ӧ�������е������������������е������� |
���� A����H��0Ϊ���ȷ�Ӧ��
B����Ӧ�ȵĴ�Сȡ���ڷ�Ӧ��ϵ��ʼ̬����̬��������أ�
C��ȼ������ָ1mol��ȼ����ȫȼ�������ȶ���������ų���������
D����Ӧ�ȣ���H��=�������������-��Ӧ�����������
��� �⣺A����H��0Ϊ���ȷ�Ӧ��������HΪ��ֵʱ����ʾ�÷�ӦΪ���ȷ�Ӧ����A����
B����Ӧ�ȵĴ�Сȡ���ڷ�Ӧ��ϵ��ʼ̬����̬��������أ���ѭ�����غ㶨�ɣ���B��ȷ��
C��H2S��ȼ���ȡ�H=-a kJ•mol-1�����ʾH2Sȼ���ȵ��Ȼ�ѧ����ʽΪH2S��g��+$\frac{3}{2}$O2��g���TSO2��g��+H2O��l����H=-a kJ•mol-1����C����
D����Ӧ�ȣ���H��=�������������-��Ӧ�������������Ӧ�ȵĴ�С�뷴Ӧ�������е���������������е������йأ���D����
��ѡB��
���� ���⿼���˷�Ӧ�ȵĺ��塢ȼ���ȡ����ȷ�Ӧ�����ȷ�Ӧ����dz����ķ��ȷ�Ӧ�����ȷ�Ӧ�������H�ĺ����ǽ��Ĺؼ�����Ŀ�ϼ�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
8�������������������Ӧ����ȷ���ǣ�������
| A�� | �ռ��NaOH | B�� | ��ʯ�� CaO | C�� | ��� Na2CO3 | D�� | С�մ� NaHCO3 |
9����ͼ��ʾ��һ���ۺϴ���SO2�����Ĺ������̣���ÿ������ȫ��Ӧ������˵����ȷ���ǣ�������
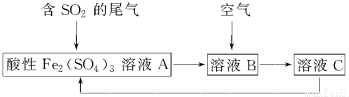

| A�� | ��ҺB�з����ķ�ӦΪ2SO2+O2�T2SO3 | |
| B�� | �������Ը��������Һ������ҺC���Ƿ���Fe3+ | |
| C�� | ���������̿���֪�����ԣ�Fe3+��O2��SO42- | |
| D�� | �˹��յ��ŵ�֮һ��������ѭ������ |
6��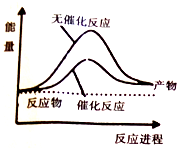 ��֪��CO��g��+2H2��g��?CH3OH��l����H=-248kJ/mol������1mol CH3OH��l����Ҫ���յ�����Ϊ157kJ�������������
��֪��CO��g��+2H2��g��?CH3OH��l����H=-248kJ/mol������1mol CH3OH��l����Ҫ���յ�����Ϊ157kJ�������������
һ�������£������1L���ܱ������м���1mol CO��g����2mol H2��g����ַ�Ӧ������CH3OH��g���ų�����Q kJ������˵����ȷ���ǣ�������
 ��֪��CO��g��+2H2��g��?CH3OH��l����H=-248kJ/mol������1mol CH3OH��l����Ҫ���յ�����Ϊ157kJ�������������
��֪��CO��g��+2H2��g��?CH3OH��l����H=-248kJ/mol������1mol CH3OH��l����Ҫ���յ�����Ϊ157kJ�������������| H2��g�� | CO��g�� | CH3OH��g�� | |
| 1mol�����еĻ�ѧ���γ�ʱҪ�ͷų�������/kJ | 436 | 1084 | a |
| A�� | ��ͼ�ɱ�ʾ�ϳɼ״������е������仯 | |
| B�� | a����ֵΪ2047 | |
| C�� | Q����ֵΪ91 | |
| D�� | ����������ͬ����Ӧʹ�ô���ʱ�ͷų���������������ʱ�ͷų������� |
13������˵����ȷ���ǣ�������
| A�� | ��ԭ�ӵ��������ǵ������ԭ������ | |
| B�� | ������Ħ��������8g•mol-1 | |
| C�� | 1molH2SO4�к�1molH2 | |
| D�� | 1molH2O��������18g |
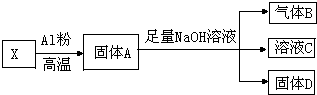 ijͬѧ���ʵ�齫Fe3O4��CuO��ɵĻ����X������ͼ��ʾ��ת����ÿһ������Ӧ��ȫ��
ijͬѧ���ʵ�齫Fe3O4��CuO��ɵĻ����X������ͼ��ʾ��ת����ÿһ������Ӧ��ȫ��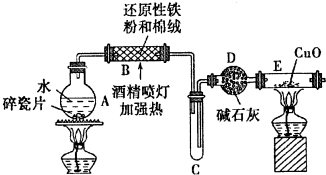
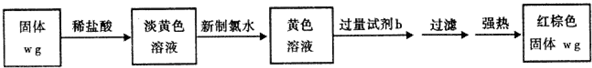
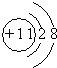 ��
��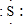 ��E���ӵķ���ΪCl-��
��E���ӵķ���ΪCl-��