题目内容
下列对几种常见的金属防腐方法的描述错误的是( )
| 选 项 | 方 法 | 对 相 应 方 法 的 描 述 |
| A | 改变金属内部的组成结构 | 此法实际上是将金属制成合金,增强抗腐蚀能力 |
| B | 在金属表面覆盖保护层 | 保护层破损后,就完全失去了对金属的保护作用 |
| C | 外加电流的阴极保护法 | 接外加直流电源构成电解池,被保护的金属作阴极 |
| D | 牺牲阳极的阴极保护法 | 构成原电池,被保护的金属作正极 |
| A、A | B、B | C、C | D、D |
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:金属的防护措施有牺牲阳极的阴极保护法、外加电流的阴极保护法,另外还有电镀、喷镀、喷油漆等方法使金属与空气、水等物质隔离,制成合金,改变金属的内部结构以防止金属腐蚀.
解答:
解:A.将金属制成合金,变金属内部的组成结构,防止金属腐蚀,例如在钢铁中加入镍和铬制成不锈钢,故A正确;
B.铁上镀锌,可以保护铁不被腐蚀,当保护层破坏以后,铁与锌在电解质环境下形成原电池,锌活泼性强于铁,做负极,铁做正极,铁受到保护,故B错误;
C.外加电流的阴极保护法,应用电解原理,被保护的金属做阴极接电源的负极,电极上发生还原反应,金属受到保护,故C正确;
D.牺牲阳极的阴极保护法,是利用原电池原理,被保护的金属作正极,故D正确;
故选:B.
B.铁上镀锌,可以保护铁不被腐蚀,当保护层破坏以后,铁与锌在电解质环境下形成原电池,锌活泼性强于铁,做负极,铁做正极,铁受到保护,故B错误;
C.外加电流的阴极保护法,应用电解原理,被保护的金属做阴极接电源的负极,电极上发生还原反应,金属受到保护,故C正确;
D.牺牲阳极的阴极保护法,是利用原电池原理,被保护的金属作正极,故D正确;
故选:B.
点评:本题考查了金属的腐蚀与防护,难度不大,注意理解各种防腐方法的原理是解题关键.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
下列离子方程式书写正确的是( )
| A、FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+═4Fe3++2H2O |
| B、碳酸钙与醋酸反应 CaCO3+2H+═Ca2++CO2↑+H2O |
| C、向Fe(NO3)3溶液中加入过量的HI溶液 2NO3-+8H++6I-═3I2+2NO↑+4H2O |
| D、向NH4HCO3溶液中加入足量NaAlO2溶液:NH4++AlO2-+2H2O=NH3?H2O+Al(OH)3↓ |
在一定温度下某密闭容器中,可逆反应A(g)+3B(g)?2C(g)+2D(s)达到平衡,下列描述一定正确的是( )
①C的生成速率与C的分解速率相等 ②单位时间内生成amolA,同时生成3amolB
③A、B、C的浓度不再变化 ④反应物的转化率不再变化
⑤混合气体的压强不再变化 ⑥混合气体的物质的量不再变化
⑦单位时间内消耗amolA,同时生成 3amolB ⑧A、B、C、D的分子数之比为1:3:2:2.
①C的生成速率与C的分解速率相等 ②单位时间内生成amolA,同时生成3amolB
③A、B、C的浓度不再变化 ④反应物的转化率不再变化
⑤混合气体的压强不再变化 ⑥混合气体的物质的量不再变化
⑦单位时间内消耗amolA,同时生成 3amolB ⑧A、B、C、D的分子数之比为1:3:2:2.
| A、①②③④⑤⑥⑦ |
| B、①③④⑤⑥⑦ |
| C、①③④⑥⑦ |
| D、①③⑤⑥⑦⑧ |
下列实验操作与安全事故处理正确的是( )
| A、除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤 | ||
| B、用点燃的火柴在液化气钢瓶口检验是否漏气 | ||
C、用试管夹从试管底由下往上夹住距离管口约
| ||
| D、把玻管插入橡胶塞孔时,用厚布护手,紧握用水湿润的玻管插入端,缓慢旋进塞孔中 |
意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子,下列说法正确的是( )
| A、N4属于一种新型的化合物 |
| B、N4与N2的摩尔质量相等 |
| C、等质量的N4与N2所含的原子个数比为1:1 |
| D、等质量的N4与N2所含的原子个数比为2:1 |
与元素的化学性质关系最密切的是( )
| A、质子数 | B、中子数 |
| C、核电荷数 | D、最外层电子数 |
下列有关实验现象的描述或实验操作的叙述正确的是( )
A、 实验室常用如图所示的装置制取少量的乙酸乙酯 |
| B、用热的纯碱溶液洗涤试管内壁附着的油脂 |
| C、棉花在酒精灯的火焰上灼烧后会产生烧焦羽毛味 |
| D、用苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出 |
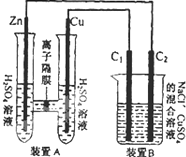 有如图装置,回答下列问题:
有如图装置,回答下列问题: