题目内容
9.表中对应关系正确的是( )| A | ①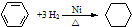 ;② ;②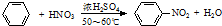 | 均为加成反应 |
| B | ①CH3CH3+Cl2$\stackrel{光}{→}$CH3CH2Cl+HCl;②CH2═CH2+HCl→CH3CH2Cl | 均为取代反应 |
| C | ①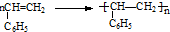 ;②6CO2+6H2O$→_{叶绿素}^{光}$C6H12O6+6O2 ;②6CO2+6H2O$→_{叶绿素}^{光}$C6H12O6+6O2 | 均为加聚反应 |
| D | ①C(s)+CO2(g)═2CO(g) ②2NH4Cl(s)+Ba(OH)2•8H2O(s)═BaCl2(s)+2NH3(g)+10H2O(l) | 均为△H>0的反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.苯与浓硝酸发生取代反应;
B.乙烯与HCl发生加成反应;
C.二氧化碳生成葡萄糖的反应不是加聚反应;
D.两种反应都吸收热量,为吸热反应.
解答 解:A.苯与氢气的反应为加成反应,而与浓硝酸发生取代反应,故A错误;
B.乙烷与氯气的反应为取代反应,而乙烯与HCl发生加成反应,故B错误;
C.葡萄糖不是高聚物,二氧化碳生成葡萄糖的反应不是加聚反应,故C错误;
D.两种反应都吸收热量,为吸热反应,故D正确.
故选D.
点评 本题考查有机物的结构和性质,侧重于考查化学反应类型的判断,注意把握有机物官能团的变化,难度不大.

练习册系列答案
相关题目
20.某烷烃分子量为72,跟氯气反应生成的一氯代物只有一种,该烷烃的结构简式是( )
| A. | CH3CH2CH3 | B. |  | C. |  | D. |  |
17.4-溴甲基-1-环已烯的一种合成路线如下:

下列说法正确的是( )

下列说法正确的是( )
| A. | 化合物X、Y、Z中均有一个手性碳原子 | |
| B. | ①、②、③的反应类型依次为加成反应、还原反应和取代反应 | |
| C. | 由化合物Z一步制备化合物Y的转化条件是:NaOH醇溶液,加热 | |
| D. | 化合物Y先经酸性高锰酸钾溶液氧化,再与乙醇在浓硫酸催化下酯化可制得化合物X |
4.某导电性塑料的结构如图所示,合成该塑料的单体为( )

| A. | 乙炔 | B. | 乙烯 | C. | 乙烷 | D. | 甲烷 |
14.H2O2是实验室常见的强氧化剂,在医疗上可用作消毒剂等.

(1)实验室可用Na2O2与H2SO4反应制取少量的H2O2,Na2O2的电子式为 .
.
(2)一种正在开发的利用O2和H2O作原料通过化合制取H2O2的方法,其原理如1图所示.该方法制取H2O2
的总化学反应方程式为O2+2H2O$\frac{\underline{\;电解\;}}{\;}$2H2O2
(3)医疗上可用质量分数为3%过氧化氢溶液对伤口进行消毒,其消毒原理是H2O2使病毒蛋白质发生变性,失去活性.
(4)为探究外界条件对H2O2分解化学反应速率的影响,相关实验设计如表所示:
填写表中缺少的内容:Ⅱ12%;Ⅲ1.0;Ⅳ催化剂对反应速率的影响.
(5)由铂(Pt)和金(Au)组成的纳米棒放入H2O2溶液中(如下图),纳米棒将发生定向移动.
则:Au一侧为电池的正极(选填:“正”或“负”);纳米棒向右(选填:“左”或“右”)移动.
(6)断裂1mol过氧化氢中的O-O键和氧气中的O=O键所需的能量依次分别为142kJ•mol-1、497.3kJ•mol-1.则反应2H2O2(l)═2H2O(l)+O2(g)△H=-213.3kJ•mol-1.

(1)实验室可用Na2O2与H2SO4反应制取少量的H2O2,Na2O2的电子式为
 .
.(2)一种正在开发的利用O2和H2O作原料通过化合制取H2O2的方法,其原理如1图所示.该方法制取H2O2
的总化学反应方程式为O2+2H2O$\frac{\underline{\;电解\;}}{\;}$2H2O2
(3)医疗上可用质量分数为3%过氧化氢溶液对伤口进行消毒,其消毒原理是H2O2使病毒蛋白质发生变性,失去活性.
(4)为探究外界条件对H2O2分解化学反应速率的影响,相关实验设计如表所示:
| 试管 编号 | 实验目的 | H2O2溶液 | 温度 | 水的 体积/mL | FeCl3溶液体积/mL | |
| 质量 分数 | 体积/mL | |||||
| Ⅰ | 为编号Ⅱ实验参照 | 12% | 5.0 | 常温 | 0 | 0 |
| Ⅱ | 温度对反应速率的影响 | 5.0 | 60℃ | 0 | 0 | |
| Ⅲ | 为编号Ⅳ实验参照 | 4.0% | 5.0 | 常温 | 0 | |
| Ⅳ | 4.0% | 5.0 | 常温 | 0 | 1.0 | |
(5)由铂(Pt)和金(Au)组成的纳米棒放入H2O2溶液中(如下图),纳米棒将发生定向移动.
则:Au一侧为电池的正极(选填:“正”或“负”);纳米棒向右(选填:“左”或“右”)移动.
(6)断裂1mol过氧化氢中的O-O键和氧气中的O=O键所需的能量依次分别为142kJ•mol-1、497.3kJ•mol-1.则反应2H2O2(l)═2H2O(l)+O2(g)△H=-213.3kJ•mol-1.
1.设N A代表阿伏加德罗常数,下列叙述中不正确的是( )
| A. | 在 28 g 聚乙烯树脂中,含有的碳原子个数为2N A | |
| B. | 在合成 28 g 聚乙烯树脂的单体中,含有的双键数目为N A | |
| C. | 28 g 聚乙烯树脂完全燃烧时,转移的电子数目为3N A | |
| D. | 28 g 聚乙烯树脂中,含有的C-H的数目为4N A |
19.某原电池结构如图所示,下列有关该装置的说法正确的是( )
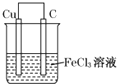

| A. | 将电能转换成化学能 | |
| B. | 碳棒上发生氧化反应 | |
| C. | 溶液中Cl-向铜棒一极移动 | |
| D. | 发生的总反应为:3Cu+2Fe3+═2Fe+3Cu2+ |