题目内容
19.某原电池结构如图所示,下列有关该装置的说法正确的是( )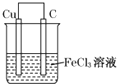
| A. | 将电能转换成化学能 | |
| B. | 碳棒上发生氧化反应 | |
| C. | 溶液中Cl-向铜棒一极移动 | |
| D. | 发生的总反应为:3Cu+2Fe3+═2Fe+3Cu2+ |
分析 因铜与铁离子可发生Cu+2Fe3+═2Fe2++Cu2+,形成原电池时,铜为负极被氧化,C为正极,Fe3+被还原生成Fe2+,电子从负极经外电路流向正极,电解质里的阳离子移向正极,阴离子移向负极,以此解答.
解答 解:A.该装置为原电池装置,可将化学能转化为电能,故A错误;
B.碳棒为正极,发生还原反应,故B错误;
C.溶液中Cl-向负极移动,即向铜棒一极移动,故C正确;
D.负极是铜失电子发生氧化反应,电极反应为Cu-2e-=Cu2+,正极反应为Fe3++e-=Fe2+,总反应为Cu+2Fe3+═2Fe2++Cu2+,故D错误;
故选C.
点评 本题考查原电池知识,为高频考点,侧重于学生的分析能力的考查,注意把握原电池的组成条件、工作原理以及电极方程式的书写,难度不大.

练习册系列答案
相关题目
9.表中对应关系正确的是( )
| A | ①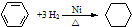 ;② ;②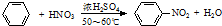 | 均为加成反应 |
| B | ①CH3CH3+Cl2$\stackrel{光}{→}$CH3CH2Cl+HCl;②CH2═CH2+HCl→CH3CH2Cl | 均为取代反应 |
| C | ①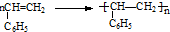 ;②6CO2+6H2O$→_{叶绿素}^{光}$C6H12O6+6O2 ;②6CO2+6H2O$→_{叶绿素}^{光}$C6H12O6+6O2 | 均为加聚反应 |
| D | ①C(s)+CO2(g)═2CO(g) ②2NH4Cl(s)+Ba(OH)2•8H2O(s)═BaCl2(s)+2NH3(g)+10H2O(l) | 均为△H>0的反应 |
| A. | A | B. | B | C. | C | D. | D |
10.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 1 mol聚乙烯含有的原子数目为6NA | |
| B. | 20℃时,1 L己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA | |
| C. | 1 mol甲基含10 NA个电子 | |
| D. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
7.我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务.下列有关海水综合利用的说法不正确的是( )
| A. | 从海水中提炼出的氘(含 HDO 0.03‰)进行核聚变,放出巨大的能量以解决能源问题, 成为一条新的科学思路.HDO与 H2O化学性质相同 | |
| B. | 从海水中提取镁可以采用下列方法:海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{HCl}{→}$MgCl2溶液→MgCl2•6H2O$→_{△}^{HCl}$MgCl2(熔融)$\stackrel{电解}{→}$Mg | |
| C. | 从海水获得的碘,可以跟氧气反应生成多种化合物,其中一种称为碘酸碘,已知该化合物中碘元素呈+3和+5两种价态,则这种化合物的化学式是 I4O9 | |
| D. | 除去粗盐中的 SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
14.设NA是阿伏加德罗常数的数值.下列说法正确的是( )
| A. | NA个Fe(OH)3胶体粒子的质量为107g | |
| B. | 常温常压下,19 g D3O+含有10 NA个电子 | |
| C. | 0.1mol氧气参加反应得到电子的数目一定为0.4NA | |
| D. | 常温下,1L0.1mol•L-1的碳酸钠溶液中含有的阴离子数大于0.1NA |
4. 某有机物的结构如图所示,它不可能具有的性质是( )
某有机物的结构如图所示,它不可能具有的性质是( )
①可以燃烧;②能使酸性KMnO4溶液褪色;③能跟NaOH溶液反应;④能发生酯化反应;⑤能发生加聚反应;⑥能发生水解反应.
 某有机物的结构如图所示,它不可能具有的性质是( )
某有机物的结构如图所示,它不可能具有的性质是( )①可以燃烧;②能使酸性KMnO4溶液褪色;③能跟NaOH溶液反应;④能发生酯化反应;⑤能发生加聚反应;⑥能发生水解反应.
| A. | ①④⑤ | B. | 只有⑥ | C. | 只有⑤⑥ | D. | ④⑤⑥ |
11.下列说法中,正确的是( )
| A. | 多糖是很多个单糖分子按照一定的方式,通过分子内脱水而结合成的 | |
| B. | 多糖在性质上跟单糖、双糖不同,通常不溶于水,没有甜味,没有还原性 | |
| C. | 淀粉和纤维素都是重要的多糖,它们的通式都是(C6H10O5)n,二者互为同分异构体 | |
| D. | 淀粉在稀H2SO4作用下水解最后生成葡萄糖和果糖 |
8.下列情况下,含微粒数目最少的是( )
| A. | 1molH2中的氢原子数 | B. | 1molOH-中的电子总数 | ||
| C. | 1molHNO3中的氧原子数 | D. | 1molH2SO4溶于水后的离子总数 |
17.下列说法正确的是( )
| A. | 将22.4 L HCl溶于水配制1 L溶液,其溶质的物质的量浓度为1.0 mol/L | |
| B. | 1 mol/L的Na2CO3溶液中含有2 mol Na+ | |
| C. | 500 mL 0.5 mol/L的(NH4)2SO4溶液中含有NH4+个数为0.5NA(NA为阿伏加德罗常数) | |
| D. | Na+浓度为0.2 mol/L的Na2SO4溶液中SO42-浓度为0.1 mol/L |