题目内容
14.已知氨可以与灼热的氧化铜反应得到氮气和金属铜:3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O,C中的现象是黑色粉末逐渐变为红色,用示意图中的装置可以实现该反应.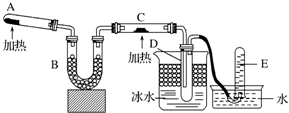
(1)A中装有Ca(OH)2和NH4Cl混合粉末,该反应的化学方程式是:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(2)B中加入的是碱石灰,其作用是干燥NH3.
(3)D中收集到的物质是氨水,检验该物质的方法将红色石蕊试纸、无水硫酸铜分别放入盛有少量的D中收集的物质的试管中现象是石蕊变蓝,白色固体变蓝.
分析 本题考查氨气的实验室制备和氨气性质检验,通过装置A加热固体氯化铵与氢氧化钙制取氨气,B为干燥氨气的装置,依据氨气的性质选择干燥剂,C装置中氨气还原氧化铜反应生成铜、氮气和水,氨气易液化,极易吸收水成为氨水,氨水具有碱性,能使红色石蕊试纸变蓝,其中的结晶水会使无水硫酸铜变蓝.
解答 解;(1)加热固体氢氧化钙和氯化铵生成氨气、氯化钙和水,化学方程式:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2 H2O;
故答案为:Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2 H2O;
(2)气体通入C中前应进行干燥,氨气为碱性气体,应选择碱性干燥剂,可以用碱石灰碱性干燥;
故答案为:干燥 NH3;
(3)氨气还原氧化铜之后剩余的氨气和产生的水蒸气在冷凝时会形成氨水,具有氨气分子和结晶水的成分,氨水可以使使红色石蕊试纸变蓝,其中的结晶水会使无水硫酸铜变蓝,
故答案为:氨水;将红色石蕊试纸、无水硫酸铜分别放入盛有少量的D中收集的物质的试管中;石蕊变蓝,白色固体变蓝.
点评 本题考查学生氨气的实验室制法、干燥以及氨气的还原性方面的知识,熟悉氨气制备原理和氨气的性质是解题 关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.下列设计的实验方案能达到实验目的是( )
| A. | 用新制Cu(OH)2悬浊液检验乙醛:向10ml10%的硫酸铜溶液中加的2%NaOH溶液4-6滴,振荡后加入乙醛溶液0.5ml,加热 | |
| B. | 探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象 | |
| C. | 向盛有过量苯酚浓溶液的试管里逐滴加入稀溴水,边加边振荡,观察三溴苯酚的生成 | |
| D. | 提纯含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入过量饱和氢氧化钠溶液,振荡后静置分液,并除去有机层的水 |
2.下面不能由单质直接化合而得到的化合物( )
| A. | FeCl2 | B. | AlCl3 | C. | FeS | D. | Fe3O4 |
9.根据反应:2FeCl3+2KI=2FeCl2+2KCl+I2;2FeCl2+Cl2=2FeCl3.判断下列物质的氧化性由强到弱的顺序是( )
| A. | Cl2>Fe3+>I2 | B. | Fe3+>Cl2>I2 | C. | Fe3+>I2>Cl2 | D. | Cl2>I2>Fe3+ |
19.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | Cl2 | B. | BaSO4 | C. | SO2 | D. | CH3COOH |
6. 污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
Ⅰ.实验原理:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O.
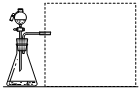
Ⅱ.实验设计(1)【方案一】测量气体产物:在相同温度下,利用右图装置,测定不同浓度H2C2O4溶液与KMnO4反应产生相同体积CO2所需的时间(忽略CO2溶解性的影响).
上图方框中应选择①②④⑤⑥(填编号)仪器组装量气装置,限选以下仪器:①广口瓶、②双孔塞、③水槽、④橡胶管、⑤导管、⑥量筒.
(2)【方案二】观察反应现象:在其它相同条件下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4溶液混合后,溶液褪色所需的时间.拟定实验数据:表中①、②处的数据
分别是5.0、25.
Ⅲ.讨论与交流:(3)实验室常用KMnO4标准溶液滴定某浓度草酸.KMnO4溶液置于酸式
酸式滴定管(填“酸式”或“碱式”)中,判断到达滴定终点的现象
是当滴入最后一滴KMnO4溶液时,溶液由无色变为浅紫红色,且半分钟内不褪色.若读取滴定管数据时,起始读数正确,终点俯视读数,则测定结果偏低(填“偏高”、“偏低”、“无影响”).
 污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.Ⅰ.实验原理:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O.
Ⅱ.实验设计(1)【方案一】测量气体产物:在相同温度下,利用右图装置,测定不同浓度H2C2O4溶液与KMnO4反应产生相同体积CO2所需的时间(忽略CO2溶解性的影响).
上图方框中应选择①②④⑤⑥(填编号)仪器组装量气装置,限选以下仪器:①广口瓶、②双孔塞、③水槽、④橡胶管、⑤导管、⑥量筒.
(2)【方案二】观察反应现象:在其它相同条件下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4溶液混合后,溶液褪色所需的时间.拟定实验数据:表中①、②处的数据
| 实验序号 | 温度/℃ | 各物质的体积/mL | 反应时间 | |||
| H2O | 3mol/L稀硫酸 | 0.1mol/L KMnO4溶液 | 0.6mol/LH2C2O4溶液 | |||
| 1 | 25 | 3.0 | 2.0 | 4.0 | 6.0 | t1 |
| 2 | 25 | ① | 2.0 | 4.0 | 4.0 | t2 |
| 3 | ② | 7.0 | 2.0 | 4.0 | 2.0 | t3 |
Ⅲ.讨论与交流:(3)实验室常用KMnO4标准溶液滴定某浓度草酸.KMnO4溶液置于酸式
酸式滴定管(填“酸式”或“碱式”)中,判断到达滴定终点的现象
是当滴入最后一滴KMnO4溶液时,溶液由无色变为浅紫红色,且半分钟内不褪色.若读取滴定管数据时,起始读数正确,终点俯视读数,则测定结果偏低(填“偏高”、“偏低”、“无影响”).
3.琥珀酸与乙醇反应生成琥珀酸二乙酯(结构如图所示),下列有关说法正确的是( )
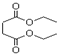

| A. | 1mol琥珀酸二乙酯能与4mol的NaOH反应 | |
| B. | 琥珀酸二乙酯在一定条件下能发生取代、加成和氧化反应 | |
| C. | 琥珀酸的分子式为C4H8O4 | |
| D. | 琥珀酸分子中含有六元环 |
4.下列过程中,一定需要通电才能实现的是( )
| A. | 电解质电离 | B. | 电化学防腐 | C. | 蓄电池放电 | D. | 电解精炼铜 |
 .
.