题目内容
10.苯加溴水后,振荡,溴水层颜色变浅,这是由于( )| A. | 溴挥发了 | B. | 发生了取代反应 | C. | 发生了萃取 | D. | 发生了加成反应 |
分析 苯和溴水不反应,苯苯溶于水,溴易溶于苯,溶液分层,以此解答该题.
解答 解:由于苯分子中碳碳化学键是介于单键和双键之间的独特的键,分子中没有碳碳双键,不能与溴水发生加成反应,
没有催化剂存在,且必须是液溴,不能使用溴水,所以溴水和苯不发生取代反应;
将浓溴水加入苯中,溴水的颜色变浅,根据相似相容原理,溴单质易溶于苯,苯能萃取溴水中的溴而使溴水褪色,发生的是萃取作用,
故选C.
点评 本题考查了苯的结构和化学性质,为高频考点,题目难度不大,注意掌握苯的结构及性质,明确溴和苯反应,必须存在催化剂,且必须使用液溴,不能使用溴水.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
17.下列各物质只用水不能将其鉴别出来的是( )
| A. | CuSO4、Na2SO4、BaSO4三种粉末 | B. | CuSO4、(NH4)2SO4、Na2SO4三种粉末 | ||
| C. | 汽油、乙醇、四氯化碳三种液体 | D. | NaOH、NH4NO3、NaCl三种晶体. |
18.在用Zn片、Cu片和稀硫酸组成的电池装置中,经过一段时间工作后,下列说法中正确的是( )
| A. | 溶液中的阳离子向正极移动,阴离子向负极移动 | |
| B. | 电流方向是从锌片经导线流向铜片 | |
| C. | 锌片是正极,铜片上有气泡产生 | |
| D. | 电解液的酸性逐渐增强 |
15. 图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
(1)在卡片上,叙述合理的是③⑤(填序号).
(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是锌片不纯,在锌片上形成原电池.
(3)如果把锌片换成石墨,发现电流计指针几乎不能偏转,原因Cu和石墨都不与硫酸反应,不会形成原电池.
(4)如果把硫酸换成硫酸铜溶液,猜测铜极(填“锌极”或“铜极”)变粗,原因是Cu2++2e-=Cu(用电极方程式表示).
 图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:| Date:2015.03.06 实验后的记录: ①Zn为阳极,Cu为阴极 ②H+向负极移动 ③电子流动方向Zn→Cu ④Zn极有H2产生 ⑤若有1mol电子流过导线,则产生H2为0.5mol. ⑥正极的电极反应式:Zn-2e-=Zn2+ |
(2)在实验中,甲同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是锌片不纯,在锌片上形成原电池.
(3)如果把锌片换成石墨,发现电流计指针几乎不能偏转,原因Cu和石墨都不与硫酸反应,不会形成原电池.
(4)如果把硫酸换成硫酸铜溶液,猜测铜极(填“锌极”或“铜极”)变粗,原因是Cu2++2e-=Cu(用电极方程式表示).
2.若NA表示阿伏加德罗常数,下列关于0.3mol/L的MgCl2溶液的说法正确的是( )
| A. | 100毫升的溶液中含有Mg2+、Cl-总数为0.3NA | |
| B. | 100毫升的溶液中含有Mg2+数目是0.1NA | |
| C. | 1升溶液中Mg2+的浓度是0.3mol/L | |
| D. | 1.5升溶液中含有Cl-的浓度是4.5mol/L |
19. 如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,这些记录中合理的是( )
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,这些记录中合理的是( )
 如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,这些记录中合理的是( )
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,这些记录中合理的是( )| A. | 铜是负极,锌为正极 | |
| B. | 铜表面产生大量气体 | |
| C. | 正极反应式:Cu-2e-═Cu2+,发生氧化反应 | |
| D. | 导线中电子的流向是:Cu→Zn |
20.下列实验操作方法正确的是( )
| A. | 欲除去乙烷中混有的乙烯可选用酸性KMnO4溶液洗气 | |
| B. | 使用萃取的方法可提纯粗苯甲酸 | |
| C. | 欲区分苯和甲苯,分别取少量样品加足量酸性KMnO4溶液,振荡,KMnO4溶液褪色为甲苯,反之为苯 | |
| D. | 欲确定溴乙烷中含有溴原子,加入适量NaOH溶液后加热,待溶液冷却后滴加AgNO3溶液,若生成淡黄色沉淀即可确定 |
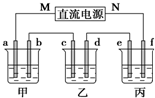 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题: