题目内容
17.核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域.已知只有质子数或中子数为奇数的原子核有NMR现象,试判断下列哪组原子均可产生NMR现象( )| A. | 18O 31P 119Sn | B. | 27Al 19F 12C | ||
| C. | 14N 17O 1H | D. | 13C ${\;}_{20}^{40}Ca$${\;}_{26}^{56}Fe$ |
分析 根据信息中只有质子数或中子数为奇数的原子核有NMR现象来分析,并利用质量数=质子数+中子数来计算.
解答 解:A.119Sn有50个质子69个中子,31P有15个质子16个中子符合题意,而18O有8个质子10个中子,故A错误;
B.27Al有27个质子30个中子,19F有9个质子10个中子符合题意,而12C有6个质子6个中子,故B错误;
C.14N有7个质子7个中子,17O有8个质子9个中子,1H有1个质子符合题意,故C正确;
D.13C有6个质子7个中子,而${\;}_{20}^{40}Ca$有20个质子20个中子,${\;}_{26}^{56}Fe$有26个质子39个中子,故D错误.
故选C.
点评 本题考查质子数中子数和质量数的关系,难度不大,注意基础知识的积累掌握.

练习册系列答案
相关题目
8.能够用键能解释的是( )
| A. | 氮气的化学性质比氧气稳定 | B. | 常温常压下,溴呈液体,碘为固体 | ||
| C. | 稀有气体一般很难发生化学反应 | D. | 硝酸易挥发,硫酸难挥发 |
5.下列物质性质的变化规律与分子间作用力有关的是( )
| A. | F2、CI2、Br2、I2的熔、沸点逐渐升高 | |
| B. | 碳化硅、晶体硅的熔、沸点很高 | |
| C. | NaF、NaCI、NaBr、NaI的熔点依次降低 | |
| D. | HF、HCI、HBr、HI的热稳定性依次 |
6.要配制浓度约为2mol/LNaOH溶液100mL,下面的操作正确的是( )
| A. | 称取8gNaOH固体,放入100mL量筒,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL | |
| B. | 称取8gNaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 | |
| C. | 称取8gNaOH固体放入300mL烧杯中,用100mL量筒量取100mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解 | |
| D. | 用50mL量筒量取50mL4mol/LNaOH溶液,倒入100mL烧杯中,再用同一量筒取50mL蒸馏水,不断搅拌下,慢慢倒入烧杯中 |
7.不能通过单质之间化合反应得到的化合物是( )
| A. | CuCl2 | B. | FeCl2 | C. | HCl | D. | Na2O2 |





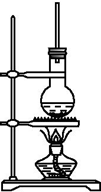 如图为硬脂酸甘油酯在碱性条件下水解的装置图.进行皂化反应时的步骤如下:
如图为硬脂酸甘油酯在碱性条件下水解的装置图.进行皂化反应时的步骤如下: