题目内容
14.某铜矿石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物.实验室以此铜矿石为原料制备CuSO4•5H2O及CaCO3,部分步骤如下: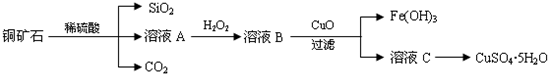
请回答下列问题:
(1)溶液A除含有Cu2+外,还可能含有的金属离子有Fe2+、Fe3+(填离子符号),验证所含离子所用的试剂是酸性高锰酸钾溶液、KSCN溶液.
(2)可用生成的CO2制取优质碳酸钙.制备时,先向氯化钙溶液中通入氨气,再通入CO2.
①实验室通常采用加热氯化铵和氢氧化钙混合物的方法制取氨气.某学习小组选取如图1所给部分装置制取并收集纯净的氨气.
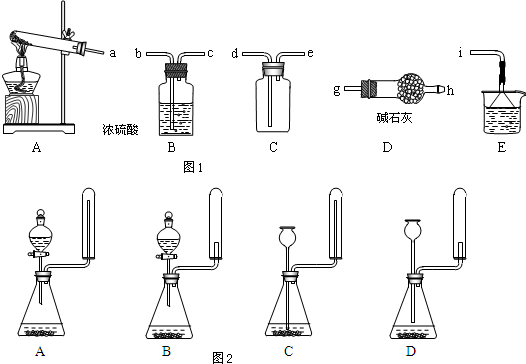
如果按气流方向连接各仪器接口,你认为正确的顺序为a→g、h→e、d→i.其中与i相连漏斗的作用是防止倒吸.
②实验室中还可用固体氢氧化钠和浓氨水制取少量氨气,图2中最适合完成该实验的简易装置是A(填编号)
(3)测定铜矿石中Cu2(OH)2CO3质量百分含量的方法是:a.将1.25g铜矿石制取的CuSO4•5H2O于锥形瓶中,加入适量水完全溶解;b.向溶液中加入100mL0.25mol/L的氢氧化钠溶液使Cu2+完全沉淀;c.过滤;d.滤液中的氢氧化钠溶液用0.5mol/L盐酸滴定至终点,耗用10mL盐酸.则铜矿石中Cu2(OH)2CO3质量分数为88.8%.
分析 Cu2(OH)2CO3以及Fe、Si的化合物与稀硫酸反应生成硫酸铜、硫酸亚铁、硫酸铁,二氧化硅与稀硫酸不反应,溶液A中加入双氧水具有强氧化性,能把亚铁离子氧化生成铁离子,所以在溶液A中加入H2O2反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O,溶液B中加入氧化铜调节溶液PH使铁离子全部沉淀,过滤得到滤液,蒸发浓缩,冷却结晶,过滤洗涤得到硫酸铜晶体,
(1)Cu2(OH)2CO3以及Fe、Si的化合物与稀硫酸反应生成硫酸铜、硫酸亚铁、硫酸铁,二氧化硅与稀硫酸不反应,所以溶液中A中除含有Cu2+外,还可能含有的金属离子有Fe2+、Fe3+,验证所含离子所用的试剂是高锰酸钾溶液检验亚铁离子,用硫氰酸钾溶液遇到铁离子形成血红色溶液,
(2)①根据装置图可知,A装置是制备氨气的.由于生成的氨气中含有水蒸气,所以需要干燥,选用碱石灰干燥.氨气的密度小于空气的,且氨气极易溶于水,所以应该用向下排空气法收集,且需要将多余的氨气进行吸收,与i相连的漏斗的作用是防止倒吸.
②用固体氢氧化钠和浓氨水制取少量氨气,因此需要分液漏斗,反应不需要加热,且氨气用向下排空气法收集;
(3)消耗盐酸的物质的量是0.01L×0.5mol/L=0.005mol,则根据方程式NaOH+HCl=NaCl+H2O可知,与盐酸反应的氢氧化钠是0.005mol.氢氧化钠的物质的量是0.1L×0.25mol/L=0.025mol,则与硫酸铜反应的氢氧化钠是0.025mol-0.005mol=0.020mol.则根据方程式2NaOH+CuSO4=Cu(OH)2↓+Na2SO4可知,硫酸铜的物质的量是0.020mol÷2=0.010mol,所以根据原子守恒可知,铜矿石中Cu2(OH)2CO3的物质的量是0.010mol÷2=0.005mol,计算得到质量分数;
解答 解:双氧水具有强氧化性,能把亚铁离子氧化生成铁离子,所以在溶液A中加入H2O2反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(1)Cu2(OH)2CO3以及Fe、Si的化合物与稀硫酸反应生成硫酸铜、硫酸亚铁、硫酸铁.二氧化硅与稀硫酸不反应,所以溶液A中除含有Cu2+外,还可能含有的金属离子有Fe2+、Fe3+,验证所含离子所用的试剂是高锰酸钾溶液检验亚铁离子,用硫氰酸钾溶液遇到铁离子形成血红色溶液,
故答案为:Fe2+、Fe3+,酸性高锰酸钾溶液、KSCN溶液;
(2)①根据装置图可知,A装置是制备氨气的.由于生成的氨气中含有水蒸气,所以需要干燥,选用碱石灰干燥.氨气的密度小于空气的,且氨气极易溶于水,所以应该用向下排空气法收集,且需要将多余的氨气进行吸收,因此正确的操作顺序是a→g、h→e、d→i;氨气极易溶于水,因此与i相连的漏斗的作用是防止倒吸,
故答案为:ghed,防止倒吸;
②用固体氢氧化钠和浓氨水制取少量氨气,因此需要分液漏斗.反应不需要加热,且氨气用向下排空气法收集,所以正确的答案选A,
故答案为:A;
(3)消耗盐酸的物质的量是0.01L×0.5mol/L=0.005mol,则根据方程式NaOH+HCl=NaCl+H2O可知,与盐酸反应的氢氧化钠是0.005mol.氢氧化钠的物质的量是0.1L×0.25mol/L=0.025mol,则与硫酸铜反应的氢氧化钠是0.025mol-0.005mol=0.020mol.则根据方程式2NaOH+CuSO4=Cu(OH)2↓+Na2SO4可知,硫酸铜的物质的量是0.020mol÷2=0.010mol,所以根据原子守恒可知,铜矿石中Cu2(OH)2CO3的物质的量是0.010mol÷2=0.005mol,所以Cu2(OH)2CO3质量分数为$\frac{0.005mol×222g/mol}{1.25g}$×100%=88.8%.
故答案为:88.8%.
点评 本题考查了混合物质的分离提纯,实验过程分析判断,注意仪器的应用和含量的计算,掌握基础是解题关键,题目难度中等.


| A. | 该物质属于芳香族化合物 | B. | 它的分子式是C16H10N2O2 | ||
| C. | 靛蓝完全燃烧生成二氧化碳和水 | D. | 它是不饱和的有机物 |
| A. | 钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀 | |
| B. | 原电池反应是导致金属腐蚀的主要原因,故不能用原电池原理来减缓金属的腐蚀 | |
| C. | 钢铁电化学腐蚀的两种类型主要区别在于水膜的酸性不同,引起的正极反应不同 | |
| D. | 无论哪种类型的腐蚀,其实质都是金属被还原 |
提示信息:
①下列四种离子完全沉淀时溶液pH值如下表:
| 金属离子 | 完全沉淀pH |
| Fe2+ | 9.7 |
| Mg2+ | 12.4 |
| Fe3+ | 3.2 |
| Al3+ | 5.2 |
回答下列问题:
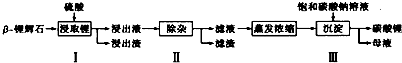
(1)步骤Ⅰ前,β锂辉石要粉碎成细颗粒的目的是增加样品与H2SO4的接触面积,加快化学反应速率.
(2)步骤Ⅰ中,酸浸后得到的酸性溶液中含有Li+、SO${\;}_{4}^{2-}$,另含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入石灰石(填“石灰石”“氯化钙”或“稀硫酸”)以调节溶液的pH到6.0~6.5,可以除去的离子有Al3+、Fe3+,然后分离得到浸出液.
(3)步骤Ⅱ中,将适量的H2O2溶液、石灰乳和Na2CO3溶液依次加入浸出液中,可除去的杂质金属离子有Fe2+、Mg2+、Ca2+.
(4)步骤Ⅲ中,生成沉淀的离子方程式为2Li++CO32-=Li2CO3↓.

艺流程如下:

请回答下列问题:
(1)碱式硫酸铁能够净水的原因是能水解生成吸附能力很强的胶体.
(2)已知,常温下部分阳离子以氢氧化物形式完全沉淀时溶液的pH如下表.假设沉淀完全时溶液中金属离子的浓度为1×10-5 mol•L-1,估算Ksp[Fe(OH)2]=1×10-15.生产碱式硫酸铁的过程中,加入少量NaHCO3
调溶液pH=6的目的是调节溶液的pH促进Al3+水解转化为沉淀完全除去.
| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Al (OH)3 |
| 开始沉淀时的pH | 7.0 | 1.9 | 3.4 |
| 完全沉淀时的pH | 9.0 | 3.2 | 4.7 |
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁.根据我国质量标准,产品中不得含有Fe2+及NO${\;}_{3}^{-}$.某同学根据提供的试剂设计实验检验所得产品中不含Fe2+,含有 SO${\;}_{4}^{2-}$,可供选择的试剂如下:
A.新制氯水 B.0.l mol/L KSCN溶液 C.10%NaOH溶液
D.20%HNO3溶液 E.0.05mol/L酸性KMnO4溶液 F.0.l mol/L BaCl2溶液
请你帮助该同学完成实验,将相关项目填入下表:
| 实验操作 | 现象 | 结论 |
| 取适量产品于洁净烧杯中,加入适量蒸馏水,充分搅拌,静置,滤去沉淀. | 得黄棕色溶液 | |
| 取少量溶液于试管中,滴加溶液 ①0.05mol/L酸性高锰酸钾; | ②溶液不褪色; | 溶液中不含Fe2+ |
| 取少量溶液于试管中,滴加0.1 mol/L BaCl2溶液,再滴加20% HNO3溶液 | ③产生白色沉淀; | 溶液中含有SO${\;}_{4}^{2-}$ |