题目内容
8.下列反应不是离子反应的是( )| A. | 氯化钠溶液中滴入硝酸银溶液 | B. | 碳在氧气中燃烧 | ||
| C. | 铁片置于硫酸铜溶液中 | D. | 氢氧化钠溶液与稀硫酸反应 |
分析 离子之间结合生成沉淀、气体、水等,则离子之间发生反应,有离子参加的反应为离子反应,以此来解答.
解答 解:A.氯离子与银离子结合生成氯化银沉淀,可发生离子反应,故A不选;
B.为固体与气体的反应,没有离子参加,不是离子反应,故B选;
C.发生Fe与铜离子的置换反应,为离子反应,故C不选;
D.氢氧根离子与氢离子结合生成水,可发生离子反应,故D不选;
故选B.
点评 本题考查离子反应及离子共存,为高频考点,把握常见离子之间的反应及离子反应的判断为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
19.元素在周期表中的位置,反映了元素的原子结构和元素的性质.
(1)下表是元素周期表的一部分,根据表中给出的8种元素,用元素符号或化学式回答下列问题:
①单质的化学性质最不活沷的元素是Ne;形成化合物种类最多的元素是C;原子半径最大的元素是Na.
②元素最高价氧化物对应水化物中,酸性最强的是HClO4.
③B与C两元素的气态氢化物,热稳定性较强的是第三周期VA族.
(2)四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
回答下列问题:
①元素Z位于周期表中第三周期VA 族.
②Y元素的原子结构示意图为 .
.
③元素X的气态氢化物与元素W的最高价氧化物对应水化物反应的生成物中化学键的类型是离子键、共价键.
(1)下表是元素周期表的一部分,根据表中给出的8种元素,用元素符号或化学式回答下列问题:
| 周期族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | A | B | C | D | ||||
| 3 | E | F | G | H |
②元素最高价氧化物对应水化物中,酸性最强的是HClO4.
③B与C两元素的气态氢化物,热稳定性较强的是第三周期VA族.
(2)四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.
| X | ||
| Y | Z | W |
①元素Z位于周期表中第三周期VA 族.
②Y元素的原子结构示意图为
 .
.③元素X的气态氢化物与元素W的最高价氧化物对应水化物反应的生成物中化学键的类型是离子键、共价键.
16.燃烧某有机物只生成二氧化碳8.8g和水2.7g,下列说法中,正确的是( )
| A. | 该有机物的最简式为C2H3 | |
| B. | 该有机物分子中肯定不含有碳碳叁键 | |
| C. | 该有机物不可能含有氧元素 | |
| D. | 该有机物不可能是丁烷 |
3.下列有关原电池的说法正确的是( )
| A. | 原电池是把电能转化为化学能的装置 | |
| B. | 原电池中电子流出的一极是负极,发生还原反应 | |
| C. | 构成原电池的两极必须是两种不同的金属 | |
| D. | Cu-Fe稀硫酸原电池工作时,铜是正极 |
13.饱和氯水久置后,溶液中的各种粒子:①Cl2 ②H+ ③Cl- ④HClO 减少的是( )
| A. | ①②④ | B. | ①②③ | C. | ①④ | D. | ②④ |
20.在NH3、H2SO4的工业生产中,具有的共同点是( )
| A. | 使用催化剂 | B. | 使用尾气吸收装置 | ||
| C. | 使用H2作原料 | D. | 使用吸收塔设备 |
17.常温下,将盐酸和一元碱MOH溶液等体积混合(忽略溶液体积变化),两种溶液的浓度和混合后所得溶液的pH如下表:下列判断错误的是( )
| 实验编号 | 盐酸的浓度(mol?L-1) | MOH溶液的浓度(mol?L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | a |
| 乙 | 0.2 | c1 | 7 |
| 丙 | 0.1 | 0.1 | 5 |
| A. | 甲组混合溶液中M+水解程度较丙组中大,且a<5 | |
| B. | 甲组混合溶液中:c(Cl-)>c(M+)>c(H+)>c(OH-) | |
| C. | 乙组混合溶液中:c(M+)+c(MOH)>0.1mol?L-1,且c1>0.2 | |
| D. | 丙组混合溶液中:c(OH-)+c(MOH)=1×10-5 mol?L-1 |
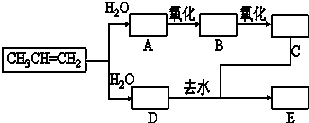 已知:①丙烯与水进行加成反应,其可能的产物有两种;②图中E为开链的酯类化合物,其分子式为C6H12O2.
已知:①丙烯与水进行加成反应,其可能的产物有两种;②图中E为开链的酯类化合物,其分子式为C6H12O2.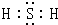 .
.