题目内容
18.X、Y、Z、M四种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.(1)Z的元素符号为Na.
(2)X2M的电子式为
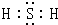 .
.(3)某燃料电池将多孔镍电极放置在KOH溶液中,然后分别向两极通入X2和Y2,即可产生电流.该电池负极的电极反应式为2H2-4e-+4OH-=4H2O,工作时,负极区溶液pH减小.(填“增大”“减小”或“不变”)
分析 X、Y、Z、M四种元素分属三个短周期,且原子序数依次增大,所以X是H元素;X、Z同主族,可形成离子化合物ZX,且Y原子序数大于Y原子序数,所以Z是Na元素;Y、M同主族,可形成MY2、MY3两种分子,所以Y是O元素,M是S元素,据此解答.
解答 解:X、Y、Z、M四种元素分属三个短周期,且原子序数依次增大,所以X是H元素;X、Z同主族,可形成离子化合物ZX,且Y原子序数大于Y原子序数,所以Z是Na元素;Y、M同主族,可形成MY2、MY3两种分子,所以Y是O元素,M是S元素,
(1)根据上面的分析可知,Z的元素符号为Na,故答案为:Na;
(2)X2M为H2S,是共价化合物,其电子式为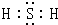 ,故答案为:
,故答案为: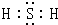 ;
;
(3)某燃料电池将多孔镍电极放置在KOH溶液中,然后分别向两极通入H2和O2,即可产生电流,在此氢氧燃烧电池中,氢气是还原剂,在电池负极发生氧化反应,反应的电极反应式为 2H2-4e-+4OH-=4H2O,由于工作时,负极区消耗氢氧根离子,所以溶液pH会减小,
故答案为:2H2-4e-+4OH-=4H2O;减小;
点评 本题以元素推断为载体考查了电子式和原电池原理等,能正确判断元素是解本题的关键,注意物质结构和化学原理知识的综合应用.

练习册系列答案
相关题目
8.下列反应不是离子反应的是( )
| A. | 氯化钠溶液中滴入硝酸银溶液 | B. | 碳在氧气中燃烧 | ||
| C. | 铁片置于硫酸铜溶液中 | D. | 氢氧化钠溶液与稀硫酸反应 |
9.下列实验目的可以实现或操作正确的是( )
| A. | 用托盘天平称取3.23 g NaCl固体 | |
| B. | 用10 mL 量筒量取 7.50 mL 稀盐酸 | |
| C. | 分液以后 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 | |
| D. | 稀释浓硫酸时,把浓硫酸沿器壁慢慢注入水里,并不断搅拌 |
13.几种短周期元素的原子半径及某些化合价见下表:
分析上表中有关数据,并结合已学过的知识,回答以下问题.涉及上述元素的答案,请用元素符号表示.
(1)E元素在周期表中位于三周期ⅥA族;
(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)F-、Na+、Al3+
(3)J单质在B单质中燃烧可生成化合物X,X的电子式是 ,其中所含的化学键类型为离子键和非极性键.
,其中所含的化学键类型为离子键和非极性键.
(4)I单质可在D的最高价氧化物中燃烧,涉及的化学方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MaO+C.
(5)B与H所形成的化合物与J的最高价氧化物对应水化物Y的溶液发生反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O.
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | +4、-2 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
(1)E元素在周期表中位于三周期ⅥA族;
(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)F-、Na+、Al3+
(3)J单质在B单质中燃烧可生成化合物X,X的电子式是
 ,其中所含的化学键类型为离子键和非极性键.
,其中所含的化学键类型为离子键和非极性键.(4)I单质可在D的最高价氧化物中燃烧,涉及的化学方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MaO+C.
(5)B与H所形成的化合物与J的最高价氧化物对应水化物Y的溶液发生反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O.
10.黄铁矿的主要成分是FeS2,FeS2读作“过硫化亚铁”,它是离子化合物,其中有类似于Na2O2结构,则下列说法中正确的是( )
| A. | 与盐酸反应的化学方程式为:FeS2+2HCl═FeCl2+S↓+H2S↑ | |
| B. | 在FeS2中,硫元素的化合价与辉铜矿(主要成分是Cu2S)中硫元素的化合价相同 | |
| C. | FeS2中的Fe元素位于第4周期第ⅧB族 | |
| D. | 若FeS2在空气中燃烧时生成Fe2O3和SO2,则1mol FeS2在反应中将失去6mol e- |
14.室温下,pH相同、体积相同的醋酸和盐酸分别采取下列措施,有关叙述正确的是( )
| A. | 加入适量醋酸钠晶体后,两溶液的pH均增大 | |
| B. | 将温度升高至50℃,两溶液的pH均不变 | |
| C. | 加水稀释至原体积的2倍后,两溶液的pH均减小 | |
| D. | 加入足量锌粉充分反应后,两溶液产生氢气一样多 |
15.2015年6月5日世界环境日的主题是“可持续消费和生产”.下列措施$\underset{不}{•}$$\underset{符}{•}$$\underset{合}{•}$其主题的是( )
| A. | 推广使用燃煤脱硫技术,防止SO2污染 | |
| B. | 采用绿色化学生产工艺,提高原子利用率 | |
| C. | 研制开发燃料电池汽车,消除机动车尾气污染 | |
| D. | 加大石油、煤炭的开采力度,增加化石燃料的供应量 |
 ,它是重要的化工原料,它在一定条件下可发生以下变化:
,它是重要的化工原料,它在一定条件下可发生以下变化:
 或
或 .
. +n NH2CH2(CH2)4CH2NH2$\stackrel{一定条件}{→}$
+n NH2CH2(CH2)4CH2NH2$\stackrel{一定条件}{→}$ +(2n-1)H2O.
+(2n-1)H2O. .
.