题目内容
9.下列排列顺序正确的是( )| A. | 热稳定性:H2O>HF>H2S | B. | 原子半径:Na>Mg>O | ||
| C. | 酸性:H3PO4>H2SO4>HClO4 | D. | 金属性:Na>Mg>Ca |
分析 A.非金属性越强,氢化物越稳定;
B.电子层越多,原子半径越大,同周期原子序数大的原子半径小;
C.非金属性越强,最高价氧化物水化物酸性越强;
D.同主族,从上到下金属性增强,结合金属活动性顺序来解答.
解答 解:A.非金属性F>O>S,氢化物的稳定性为HF>H2O>H2S,故A错误;
B.电子层越多,原子半径越大,同周期原子序数大的原子半径小,则原子半径为Na>Mg>O,故B正确;
C.非金属性Cl>S>P,最高价氧化物水化物酸性为H3PO4<H2SO4<HClO4,故C错误;
D.同主族,从上到下金属性增强,结合金属活动性顺序可知,金属性为Ca>Na>Mg,故D错误;
故选B.
点评 本题考查微粒性质的比较,为高考常见题型,侧重于学生的分析、应用能力的考查,把握元素的位置、元素周期律为解答的关键,题目难度不大.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案 课课练江苏系列答案
课课练江苏系列答案
相关题目
19.能证明某溶液中含有Fe2+的是( )
| A. | 该溶液呈浅黄色 | |
| B. | 向该溶液中加入氯水,再滴入几滴KSCN溶液,呈红色 | |
| C. | 向该溶液中滴入几滴KSCN溶液,不变色,再加入氯水,呈红色 | |
| D. | 该溶液中加入NaOH溶液,生成白色沉淀 |
20.有5种元素X、Y、Z、Q、T.X原子M层上有2个未成对电子且无空轨道;Y原子的特征电子构型为3d64s2;Z原子的L电子层的p能级上有一个空轨道;Q原子的L电子层的P能级上只有一对成对电子;T原子的M电子层上p轨道半充满.下列叙述不正确的是( )
| A. | 元素Y和Q可形成化合物Y2Q3 | |
| B. | T和Z各有一种单质的空间构型为正四面体形 | |
| C. | X和Q结合生成的化合物为离子化合物 | |
| D. | ZO2是极性键构成的非极性分子 |
14.下列说法中错误的是( )
| A. | 符合通式CnH2n+2(n≥1)且相对分子质量不相等的有机物为同系物 | |
| B. | 符合同一通式且相对分子质量不相等的有机物为同系物 | |
| C. | 乙醇和甲醚不是同系物但是同分异构体 | |
| D. | CH3CH2CHO、CH2═CHCH2OH、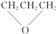 三种物质互为同分异构体 三种物质互为同分异构体 |
1.同温、同浓度下的六种溶液,其pH由小到大的顺序如下图,图中①②③代表的物质可能分别为( )
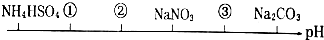
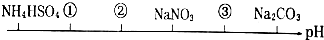
| A. | NH4Cl (NH4)2SO4 CH3COONa | B. | (NH4)2SO4 NH4Cl CH3COONa | ||
| C. | (NH4)2SO4 NH4Cl NaOH | D. | CH3COOH NH4Cl (NH4)2SO4 |
 ;结构式⑥O=C=O.
;结构式⑥O=C=O. .
. 中药在世界医学界越来越受到关注.中药药剂砒霜(主要成分As2O3)可用于治疗急性白血病,为此,砷及其化合物的提取再次引起关注.
中药在世界医学界越来越受到关注.中药药剂砒霜(主要成分As2O3)可用于治疗急性白血病,为此,砷及其化合物的提取再次引起关注. ,则其在周期表中的位置是第四周期,VA族.
,则其在周期表中的位置是第四周期,VA族.
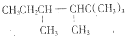 f.C8H10O2
f.C8H10O2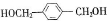 .
.