题目内容
17.在固定体积的密闭容器中,一定温度下,加入2molBr2,1molH2,发生反应:Br2(g)+H2(g)?2HBr(g),到达平衡时,HBr的浓度为W mol/L,在相同条件下,按下列情况充入物质到达平衡时,HBr的浓度仍为W mol/L的是( )| A. | 1molBr2+2molHBr | B. | 3molHBr | C. | 4molBr2+2molH2 | D. | 2molHBr |
分析 在固定体积的密闭容器中,对于Br2(g)+H2(g)?2HBr(g)反应两边计量数相等,用极端转化法,转化为相同物质的投料量之比相等,而HBr的浓度仍为W mol/L,说明是同一平衡,由此分析解答.
解答 解:在固定体积的密闭容器中,对于Br2(g)+H2(g)?2HBr(g)反应两边计量数相等,用极端转化法,转化为相同物质的投料量之比相等,而HBr的浓度仍为W mol/L,说明是同一平衡,
A、1molBr2+2molHBr转化后相当于2molBr2,1molH2,故A正确;
B、3molHBr相当于1.5molBr2,1.5molH2,故B错误;
C、4molBr2+2molH2到达平衡时,HBr的浓度为2W mol/L,故C错误;
D、2molHBr相当于1molBr2,1molH2,故D错误;
故选A.
点评 本题考查化学平衡中的等效平衡,题目难度不大,学生要学会判断等效的方法.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
7.11.6gFe3O4加到100mL某浓度的盐酸中,再加入9.8g铁粉,反应停止时,溶液中无固体存在.向溶液中滴加硫氰化钾溶液,未见颜色变化,为了中和过量的盐酸(不考虑盐酸的挥发),且使铁完全转化成Fe(OH)2,共消耗5.0mol•L-1NaOH溶液160mL.则原盐酸的物质的量浓度为( )
| A. | 2 mol•L-1 | B. | 4 mol•L-1 | C. | 6 mol•L-1 | D. | 8 mol•L-1 |
8.把0.6molX气体和0.4molY气体混合于容积为2L的容器中,使其发生如下反应:3X(g)+nY(g)?Z(g)+2W(g) 5min末生成0.2molW,消耗Y为0.1mol,则n的值为( )
| A. | 4 | B. | 3 | C. | 2 | D. | 1 |
12.下列化学实验操作或事故处理方法正确的是( )
| A. | 不慎将酸溅到眼中,应立即用氢氧化钠水溶液冲洗,边洗边眨眼睛 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸 | |
| C. | 酒精灯着火时可用水扑灭 | |
| D. | 配制硫酸溶液时,可先在量筒中加入一定量的水,再搅拌条件下慢慢加入浓硫酸 |
2.结构简式为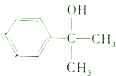 的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)( )
的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)( )
 的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)( )
的有机物在一定条件下能和氢气完全加成,加成产物的一溴代物有(不考虑-OH的取代)( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
9.取PH均等于2的盐酸和醋酸分别稀释2倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是( )
| A. | 醋酸和锌反应放出的氢气多 | |
| B. | 盐酸和醋酸分别与锌反应放出的氢气一样多 | |
| C. | 醋酸和锌反应速率较大 | |
| D. | 盐酸和醋酸分别与锌反应速率一样大 |
6.下列反应属于吸热反应的是( )
| A. | 盐酸与氢氧化钠溶液的反应 | B. | 生石灰和水的反应 | ||
| C. | 氢气在高温下与氧化铜的反应 | D. | 木炭在氧气中燃烧 |




