题目内容
下列变化中,属还原反应的是
A.Cl-→Cl2 B.FeCl2→FeCl3 C.C→CO2 D.KMnO4→MnO2
练习册系列答案
相关题目
19.下列物质在水溶液中的电离方程式书写完全正确的是( )
| A. | KMnO4=K++Mn7++4O2- | B. | Ba(OH)2═Ba2++(OH-)2 | ||
| C. | Mg(NO3)2=Mg+2+2NO3- | D. | NaHCO3═Na++HCO3- |
17.如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是( )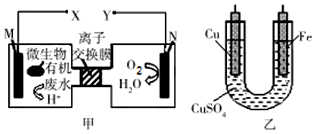

| A. | M电极反应式:(C6H10O5)n+7nH2O-24ne-═6nCO2↑+24nH+ | |
| B. | 铜电极应与X相连接 | |
| C. | 质子透过离子交换膜由右向左移动 | |
| D. | 当N电极消耗0.2 mol气体时,则铁电极增重16g |
14.已知一定温度下合成氨反应:N2+H2═2NH3 (每生成2mol NH3放出92.4kJ的热量),在恒温恒压的密闭容器中进行如下实验:①通入1mol N2和3mol H2,达平衡时放出热量为Q1,②通入2mol N2和6mol H2,达平衡时放出热量为Q2,则下列关系正确的是( )
| A. | Q2>2 Q1 | B. | Q1=92.4 kJ | C. | Q1<Q2<184.8 kJ | D. | Q1=Q2<92.4 kJ |
19.某研究性学习小组成员分别设计了如下甲、乙、丙三套实验装置制取乙酸乙酯.请回答下列问题:

(1).写出实验室制取乙酸乙酯的化学方程式CH3COOH+CH3CH2OH $?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O
(2).甲、乙、丙三套实验装置中,不宜选用的装置是丙 (填甲、乙、丙)
(3).现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图是分离操作步骤流程图,请回答.

试剂a是饱和碳酸钠溶液;分离方法①是分液,分离方法②是蒸馏.
(4).为了证明浓硫酸在反应中起到了催化剂和吸水剂的作用,某同学利用上图中某装置进行了以下4个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管乙再测有机层的厚度,实验记录如下:
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用.实验D中应加入盐酸的体积和浓度分别是3mL和4 mol•L-1.
②分析实验AC(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.

(1).写出实验室制取乙酸乙酯的化学方程式CH3COOH+CH3CH2OH $?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O
(2).甲、乙、丙三套实验装置中,不宜选用的装置是丙 (填甲、乙、丙)
(3).现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图是分离操作步骤流程图,请回答.

试剂a是饱和碳酸钠溶液;分离方法①是分液,分离方法②是蒸馏.
(4).为了证明浓硫酸在反应中起到了催化剂和吸水剂的作用,某同学利用上图中某装置进行了以下4个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管乙再测有机层的厚度,实验记录如下:
| 实验编号 | 试管甲中试剂 | 试管乙中试剂 | 有机层的厚度/cm |
| A | 2 mL乙醇、1 mL乙酸、 1mL18mol•L-1 浓硫酸 | 饱和Na2CO3溶液 | 3.0 |
| B | 2 mL乙醇、1 mL乙酸 | 0.1 | |
| C | 2 mL乙醇、1 mL乙酸、 3 mL 2mol•L-1 H2SO4 | 0.6 | |
| D | 2 mL乙醇、1 mL乙酸、盐酸 | 0.6 |
②分析实验AC(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.


 :2Ag + 2H+=2Ag+ + H2↑
:2Ag + 2H+=2Ag+ + H2↑