题目内容
3.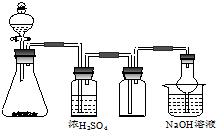 如图是一套实验室制备气体的装置,用于发生、干燥、收集和吸收有毒气体.下列各组物质能利用这套装置进行实验的是( )
如图是一套实验室制备气体的装置,用于发生、干燥、收集和吸收有毒气体.下列各组物质能利用这套装置进行实验的是( )| A. | 电石和水 | B. | 高锰酸钾和浓盐酸 | ||
| C. | Cu片和稀硝酸 | D. | FeS和稀硫酸 |
分析 由图可知,锥形瓶中为固体与液体不加热制备气体,浓硫酸干燥中性或酸性气体,集气瓶中收集密度比空气密度大的气体,最后NaOH吸收尾气且防止倒吸,以此来解答.
解答 解:A.电石和水反应生成乙炔,具有还原性,不能用浓硫酸干燥,故A错误;
B.高锰酸钾与浓盐酸在常温下反应生成氯气,可用浓硫酸干燥,且氯气可与氢氧化钠溶液反应,可用氢氧化钠溶液进行尾气吸收,故B正确;
C.铜和稀硝酸反应生成NO,NO不能用排空法收集,故C错误;
D.FeS和稀硫酸反应生成硫化氢,具有还原性,不能被浓硫酸干燥,故D错误.
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质与气体的制备实验为解答的关键,侧重分析与实验能力考查,注意制备原理及实验技能,题目难度不大.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
14.分子式为C6H12O2的有机物A,能与NaHCO3溶液产生CO2.则有机物A的可能结构有( )
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
18.下列固体加热熔化时需破坏非极性共价键的是( )
| A. | 碘单质 | B. | 金刚石 | C. | 二氧化硅 | D. | 氢氧化钠 |
15.有4.8g CuO、Fe2O3混合物与充足的CO于加热条件充分反应,反应后全部气体用0.6mol/L Ba(OH)2溶液100mL处理,有白色沉淀生成.又知反应后生成的气体质量为3.52g,下列有关叙述中正确的是( )
| A. | 原混合物中CuO与Fe2O3的质量比为2:1 | |
| B. | 生成的CO2已被Ba(OH)2溶液完全吸收,Ba2+沉淀完全 | |
| C. | 在吸收CO2后的溶液中有Ba(HCO3)2 | |
| D. | 原混合物中CuO与Fe2O3物质的量的比为l:l |
13.已知:①1molH2分子中化学键断裂时需要吸收436kJ的能量;②1molCl2分子中化学键断裂时需要吸收243kJ的能量;③由H原子和Cl原子形成1molHCl分子时释放431kJ的能量.下列叙述正确的是( )
| A. | 氢气和氯气反应生成氯化氢气体的热化学方程式为:H2(g)+Cl2(g)=2HCl(g)△H=-183kJ | |
| B. | 氢气与氯气反应生成4.48L氯化氢气体,反应的△H=-183kJ/mol | |
| C. | 氢气与氯气反应生成2mol氯化氢气体,反应的△H=+183kJ/mol | |
| D. | 氢气与氯气反应生成氯化氢气体放出183KJ的热量时,转移电子物质的量为2 mol |
 用如图所示电解装置分别完成以下要求,请填空:
用如图所示电解装置分别完成以下要求,请填空: 2-甲基戊烷
2-甲基戊烷 