题目内容
5.下列说法正确的是( )| A. | 绿色食品是不含任何化学物质的食品 | |
| B. | Na2O2与CO2反应,Na2O2是氧化剂、CO2是还原剂 | |
| C. | 向新制的FeSO4溶液中滴入适量的NaOH溶液,放置片刻,整个反应过程的颜色变化是:浅绿色溶液→白色沉淀→灰绿色沉淀→红褐色沉淀 | |
| D. | 称取等质量的两份铝粉,分别加入过量的稀盐酸和过量的NaOH溶液.则放出氢气的体积(同温同压下)不相等 |
分析 A.任何物质都是化学物质;
B.反应中只有Na2O2中的O元素变价;
C.根据铁的化合物之间的转化分析;
D.根据铝粉与酸、碱反应的方程式分析.
解答 解:A.任何物质都是化学物质,所谓绿色食品是不含对人体产生危害的化学物质的食品,故A错误;
B.在Na2O2与CO2反应中,只有Na2O2中的O元素变价,Na2O2既是氧化剂也是还原剂,故B错误;
C.会发生反应:Fe2++2OH-=Fe(OH)2↓,由于白色的Fe(OH)2不稳定,会被空气中的氧气氧化而发生反应:4Fe(OH)2+O2+2H2O=4Fe(OH)3,产生的Fe(OH)3是红褐色的,故整个反应过程的颜色变化是:浅绿色溶液→白色沉淀→灰绿色沉淀→红褐色沉淀,故C正确;
D.铝粉与酸、碱反应的方程式是:2Al+6HCl=2AlCl3+3H2↑;2Al+2NaOH+2H2O=2NaAlO2+3H2↑,由方程式可知:若两份铝粉等质量的,则在同温同压下放出氢气的体积相等,故D错误.
故选C.
点评 本题考查了氧化还原反应、铁的化合物的性质、铝的化合物的性质等,题目难度不大,侧重于基础知识的考查,注意从化合价变化的角度分析氧化还原反应.

练习册系列答案
相关题目
13.下列鉴别物质的方法能达到目的是( )
| A. | 用Ba(N03)2溶液鉴别CaCl2溶液和(NH4)2SO4溶液 | |
| B. | 用稀硫酸鉴别碳酸钠固体和碳酸钾固体 | |
| C. | 用湿润的蓝色石蕊试纸鉴别氨气和氢气 | |
| D. | 用淀汾溶液鉴别加碘盐(含KI03)和未加碘盐 |
17.1.52g 铜镁合金完全溶解于50mL 密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
| A. | 该合金中铜与镁的物质的量之比是2:1 | |
| B. | 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L | |
| C. | 得到2.54 g沉淀时,加入NaOH溶液的体积是60 mL | |
| D. | NO2和N2O4的混合气体中,NO2的体积分数是80% |
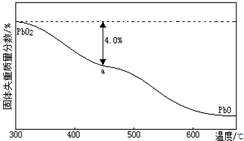 (1)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为PbO2+4HCl(浓)=PbCl2+Cl2↑+2H2O.PbO2可由PbO与次氯酸钠溶液反应制得,其反应的离子方程式为PbO+ClO-=PbO2+Cl-.
(1)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为PbO2+4HCl(浓)=PbCl2+Cl2↑+2H2O.PbO2可由PbO与次氯酸钠溶液反应制得,其反应的离子方程式为PbO+ClO-=PbO2+Cl-.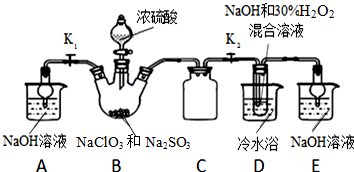

 .
.