题目内容
14.已知硼元素有两种天然同位素10B和11B,硼元素的原子量为10.80,则10B和11B的原子个数比为( )| A. | 1:4 | B. | 1:3 | C. | 1:1 | D. | 4:1 |
分析 元素的相对原子质量为该元素各种核素的相对原子质量的平均值,原子的近似相对原子质量在数值上等于其质量数,利用十字交叉法计算10B和11B的原子个数之比.
解答 解:B元素的相对原子质量10.8是质量数分别为10和11的核素的平均值,可以采用十字交叉法: ,则10B和11B的原子的个数比为0.2:0.8=1:4,
,则10B和11B的原子的个数比为0.2:0.8=1:4,
故选A.
点评 本题考查物质的量的有关计算,把握元素的相对原子质量和核素的相对原子质量之间的关系为解答的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
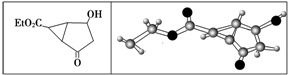
4.某化合物的结构(键线式)及球棍模型如下:
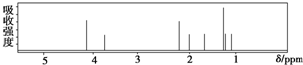
该有机物分子的1H核磁共振谱如下(单位是ppm).
下列关于该有机物的叙述不正确的是( )

该有机物分子的1H核磁共振谱如下(单位是ppm).

下列关于该有机物的叙述不正确的是( )
| A. | 该有机物分子中不同化学环境的氢原子有8种 | |
| B. | 该有机物属于芳香族化合物 | |
| C. | 键线式中的Et代表的基团为-CH2CH3 | |
| D. | 该有机物可发生水解反应 |
5.有机物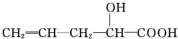 在不同条件下至少可能发生不同类型的反应:①取代反应 ②加成反应 ③消去反应 ④氧化反应 ⑤酯化反应,⑥加聚反应,其中由于其分子结构中含有-OH,可能发生的反应有( )
在不同条件下至少可能发生不同类型的反应:①取代反应 ②加成反应 ③消去反应 ④氧化反应 ⑤酯化反应,⑥加聚反应,其中由于其分子结构中含有-OH,可能发生的反应有( )
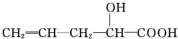 在不同条件下至少可能发生不同类型的反应:①取代反应 ②加成反应 ③消去反应 ④氧化反应 ⑤酯化反应,⑥加聚反应,其中由于其分子结构中含有-OH,可能发生的反应有( )
在不同条件下至少可能发生不同类型的反应:①取代反应 ②加成反应 ③消去反应 ④氧化反应 ⑤酯化反应,⑥加聚反应,其中由于其分子结构中含有-OH,可能发生的反应有( )| A. | ②④ | B. | ①③④⑤⑥ | C. | ②③④⑤ | D. | ①③④⑤ |
2.运用元素周期律分析下面的推断,其中正确的是( )
| A. | 第IIIA的铊(Tl)既能与盐酸作用产生氢气,又能跟NaOH溶液反应放出氢气 | |
| B. | 第VIIA的砹(At)为有色固体,易溶于四氯化碳,但难溶于水 | |
| C. | 第IIA的锶的硫酸盐(SrSO4)是易溶于水的白色固体 | |
| D. | 第VIA的硒的氢化物(H2Se)是无色、有毒,比H2S稳定的气体 |
9.下列属于氮的固定的化学反应是( )
| A. | NO与O2在反应生成NO2 | B. | 硝酸工厂用NH3氧化制NO | ||
| C. | 雷雨时空气中的N2转化为NO | D. | 由NH3制碳酸氢铵和硫酸铵 |
6.关于各装置图的叙述中,正确的是( )

| A. | 实验室用装置①制取氨气 | |
| B. | 装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 | |
| C. | 装置③可用于制备氢氧化亚铁并观察其颜色 | |
| D. | 装置④b口进气可收集CO2等气体 |
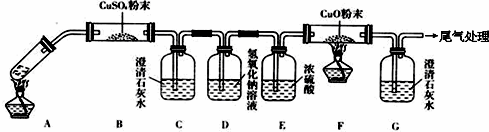
 PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、
PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、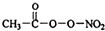 (PAN)等二次污染物.
(PAN)等二次污染物.